Table of Contents
급성 신손상
급성 신손상 (Acute Kidney Injury, AKI)
수일~수주 내 혈청 크레아티닌 상승 또는 소변량 감소
가장 흔한 원인은 신장 저관류(Prerenal)
요검사·FENa·초음파로 원인 감별
[정의]
급성 신손상은 신장이 갑자기 기능을 상실하여 노폐물과 전해질이 체내에 축적되는 상태입니다. 일반적으로 48시간 내 크레아티닌이 ≥0.3 mg/dL 증가하거나, 7일 내 기저치의 1.5배 이상 상승, 혹은 소변량이 0.5 mL/kg/h 이하로 6시간 이상 감소할 때 진단됩니다.
[원인/위험요인]
AKI 원인
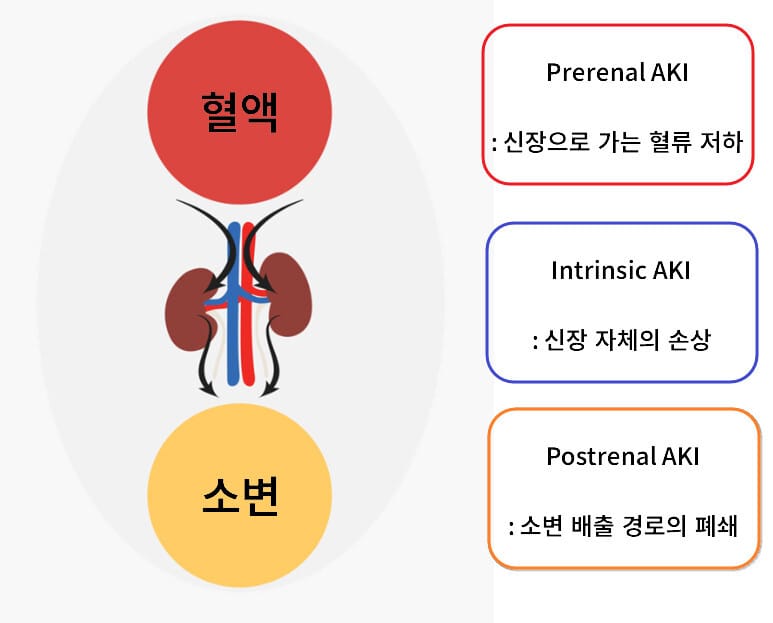
– a) Prerenal : 저관류(탈수, 출혈, 심부전)
– b) Intrinsic : 급성 세뇨관 괴사(ATN), 급성 간질성 신염(AIN), 사구체신염
– c) Postrenal : 전립선 비대, 결석, 종양
– 위험요인
> 고령, CKD 기저질환, 당뇨,
> 관련 약물 : 조영제·NSAIDs·ACEi/ARB·Aminoglycoside 사용
[임상양상]
– 소변량 감소(핍뇨, 무뇨)
– 체액 과다로 인한 부종, 폐부종, 고혈압
– 요독증: 구토, 의식 저하, 경련, 심막염
– 전해질 이상: 고칼륨혈증, 대사성 산증
[진단]
– 혈액검사: Cr, BUN 상승
– 소변검사: 침사 원주, 단백뇨 확인
– 영상: 신장 초음파로 폐쇄성 원인 배제
– FENa 측정:
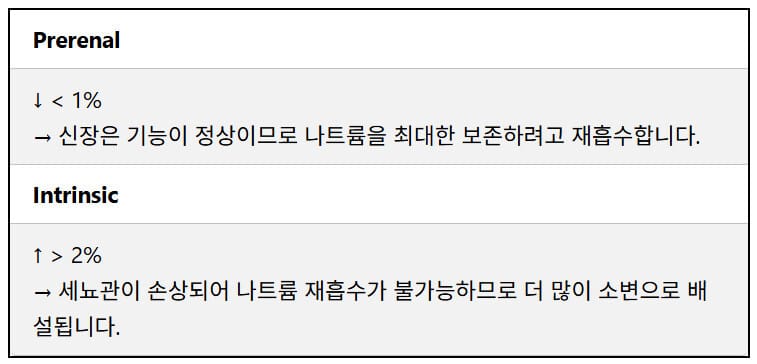
a) FeNa <1%이면 Prerenal 의심
b) FeNa > 2%이면 ATN 등 의심
[치료]
치료의 목표는 신장 관류 회복과 합병증 조절입니다.
a) 체액 부족 → 등장성 수액 보충
b) 체액 과다 → 이뇨제 사용(예후 개선은 없음)
c) 고칼륨혈증 → 칼슘제제, 인슐린/포도당, 칼륨 제거제
d) 폐쇄성 원인 → 도뇨관, 스텐트 삽입
e) 요독증·중증 전해질 이상 → 신대체요법(투석)
Prerenal AKI
[특징]
신장은 구조적으로 정상이지만 신장으로 가는 관류저하로 GFR이 감소합니다.
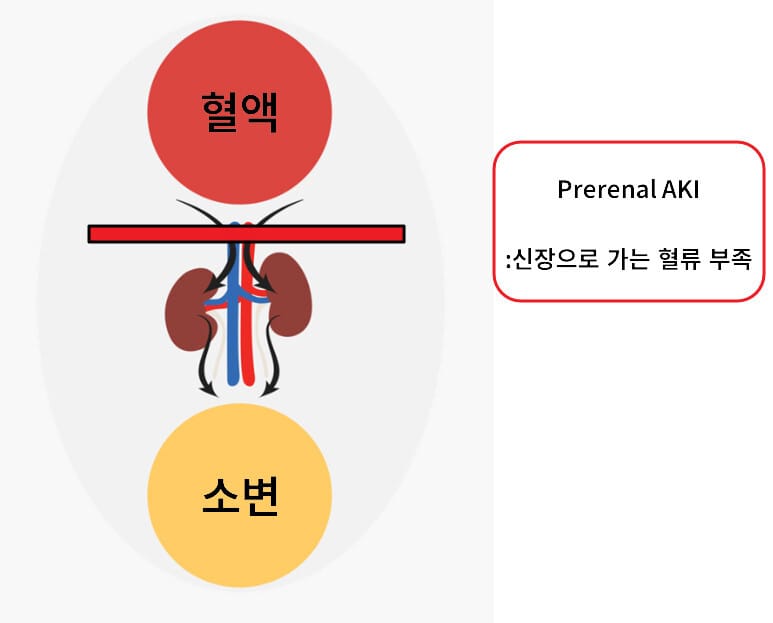
– 소변 Na 낮음
– FENa < 1% 또는 FEUrea < 35% 를 보이는 경우가 많음.
– 체액·혈역학 교정 시 가역적인 경우도 많음
FeNa (Fractional Excretion of Na⁺)
:소변 내 나트륨 배설률을 백분율로 나타낸 것으로 신장이 여과한 나트륨 중 실제로 얼마나 소변으로 배출되었는지를 확인할 수 있습니다.
– 재흡수 기능이 정상이면 FeNa는 낮고,
– 세뇨관 손상으로 재흡수가 어려우면 FeNa는 높아집니다.
[원인]
– 탈수, 출혈
– 심박출량 저하(심부전, 쇼크)
– 간경변으로 인한 신혈류 저하(hepatorenal syndrome)
[임상양상]
– 탈수에 따른 어지럼, 점막건조, 기립성 저혈압이 보일 수 있고,
– 심부전/간경변에서는 부종·복수와 함께 저나트륨혈증이 동반될 수 있습니다.
만약 이뇨제를 사용 중이면 FENa 해석이 어려워 FEUrea가 도움이 됩니다.
[치료]
– Isotonic crystalloid 수액으로 Volume 회복(출혈 시 수혈 병행).
– 심부전·간경변 등 순환장애에서는
> 혈류역학 최적화(바소프레신 유사체, 알부민 병합 등 상황별 적용)
– 신독성 약물(ACEi/ARB, NSAIDs, 아미노글리코시드, 조영제)은 일시 중지
– CT 등 영상검사를 위해 조영제가 필요할 시 수액 전처치·isotonic 조영제 를 선택합니다.
Intrinsic AKI
[특징]
신실질(세뇨관·간질·사구체·혈관)의 직접 손상.
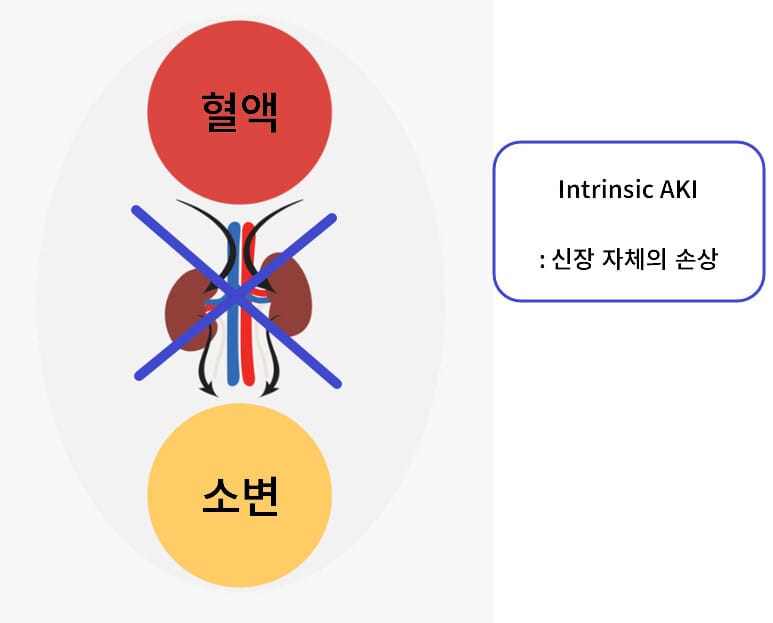
– ATN에서는 muddy brown granular casts가,
– AIN에서는 발진·발열·호산구 증가가 시사 소견입니다.
[원인]
– 급성 세뇨관 괴사(ATN): 허혈 또는 약물(아미노글리코시드, 조영제)
– 급성 간질성 신염(AIN): 약물(항생제, NSAIDs), 감염
– 사구체신염(면역학적)
– 혈관질환(혈전색전증, TMA)
[임상양상]
ATN: 허혈/독성 노출 후 수일 내 크레아티닌 상승과 비핍뇨성 또는 핍뇨성 경과가 나타납니다.
AIN: 항생제/NSAIDs 시작 1~3주 후 발열·발진·관절통, 무증상 미세혈뇨/백혈구뇨·호산구뇨가 보일 수 있습니다.
사구체신염: 혈뇨(cola-colored), 단백뇨, 고혈압, 부종이 동반됩니다.
[치료]
a) ATN
– 신독성 유발 물질 중단
– 수액, 전해질·산염기 교정,
– 수분 과다시 이뇨제로 증상 조절하되 신회복을 촉진하진 못합니다.
b) AIN
– 원인 약제 즉시 중단
– 진행/중증이면 스테로이드를 고려합니다.
c) 사구체·혈관성 원인(ANCA, anti-GBM 등)
– 면역억제(고용량 스테로이드 ± Cyclophosphamide/Rituximab )
– 혈장교환술을 병용할 수 있습니다.
급성 세뇨관 괴사 (Acute Tubular Necrosis, ATN)
AKI의 가장 흔한 원인
허혈·신독성 약물·조영제 관련
FENa 상승·과립 원주(진흙 원주)가 특징
[정의]
ATN은 허혈 또는 독성 물질에 의해 세뇨관 세포가 괴사하며 발생하는 급성 신손상의 대표적 형태입니다.
괴사된 세포와 원주가 세뇨관을 막아 여과 기능이 급격히 저하됩니다.
[원인/위험요인]
– 허혈성: 쇼크, 패혈증, 대량 출혈, 심부전 등으로 신혈류가 저하된 경우
– 독성: 아미노글리코사이드, 암포테리신B, 시스플라틴, 조영제, 중금속, 내인성 독소(미오글로빈, 헤모글로빈, 요산 등)
[임상양상]
– 무뇨/핍뇨 혹은 소변량 감소
– 체액 과다로 인한 부종·폐부종
– 전해질 이상: 고칼륨혈증·대사성 산증이 흔합니다.
[진단]
– 소변: 갈색 과립 원주(진흙 원주), 세뇨관 상피세포
– FENa > 2% (Prerenal과 감별)
– 혈액: 크레아티닌·BUN 상승
– 원인 추적 위해 영상·약력 확인 필요
[치료]
– 원인 교정이 최우선(저혈압 교정, 신독성 약물 중단)
– 체액·전해질 균형 유지
– 필요 시 투석(심한 전해질 이상·요독 증상·체액 과다)
– 예방: 고위험군에서 조영제 사용 시 수액·N-acetylcysteine 고려
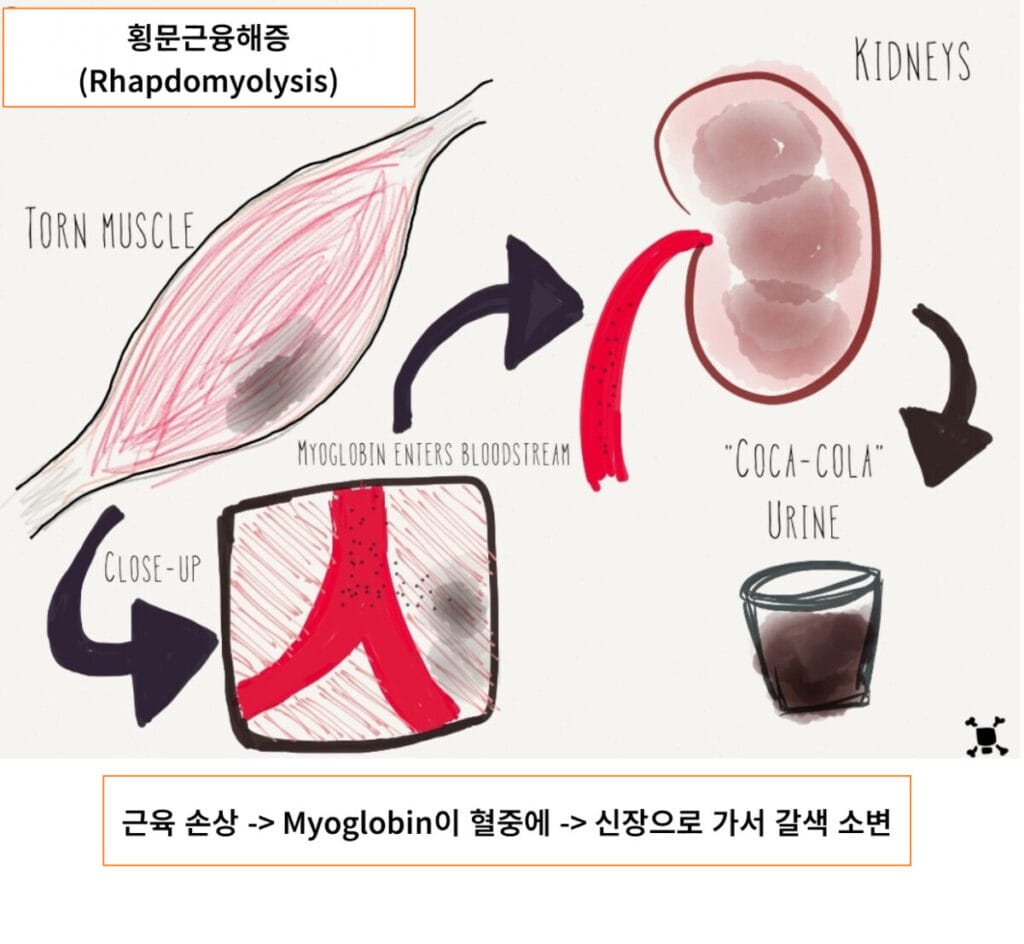
횡문근융해증 (Rhabdomyolysis)
근세포 파괴 → 미오글로빈 유리 → 세뇨관 독성·ATN
CK 현저 상승·갈색뇨(혈뇨 양성인데 RBC 적음)
조기 대량 수액이 신손상 예방의 핵심입니다
[정의]
횡문근융해증은 골격근이 급격히 파괴되며 미오글로빈·CK·칼륨·인 등이 혈중으로 유리되어 세뇨관 독성·요세관 폐색을 통해 급성 신손상(ATN)을 유발하는 상태입니다.
[원인/위험요인]
– 외상·압궤·화상·장시간 압박·경련/발작·고열/열사병이 흔한 원인입니다.
– 약물/독성: 스타틴(특히 병용: 피브레이트, CYP 억제제)·코카인·알코올·DKA 등도 관련됩니다.
– 유전성 대사근병증·감염(인플루엔자)도 드물게 원인이 됩니다.
[임상양상]
– 근통·근력저하·부종과 함께 갈색 소변이 나타날 수 있습니다.
– 고칼륨혈증·저칼슘혈증(초기)으로 부정맥·경련 위험이 있습니다.
[진단]
– 혈중 CK 현저 상승(보통 >5,000 IU/L)이 진단에 가장 민감합니다.
– 요시험지에서 혈뇨 양성이지만 현미경에 적혈구가 적은 경우가 전형적입니다.
– 전해질(칼륨↑, 인↑, 칼슘↓), 크레아티닌 상승을 확인합니다.
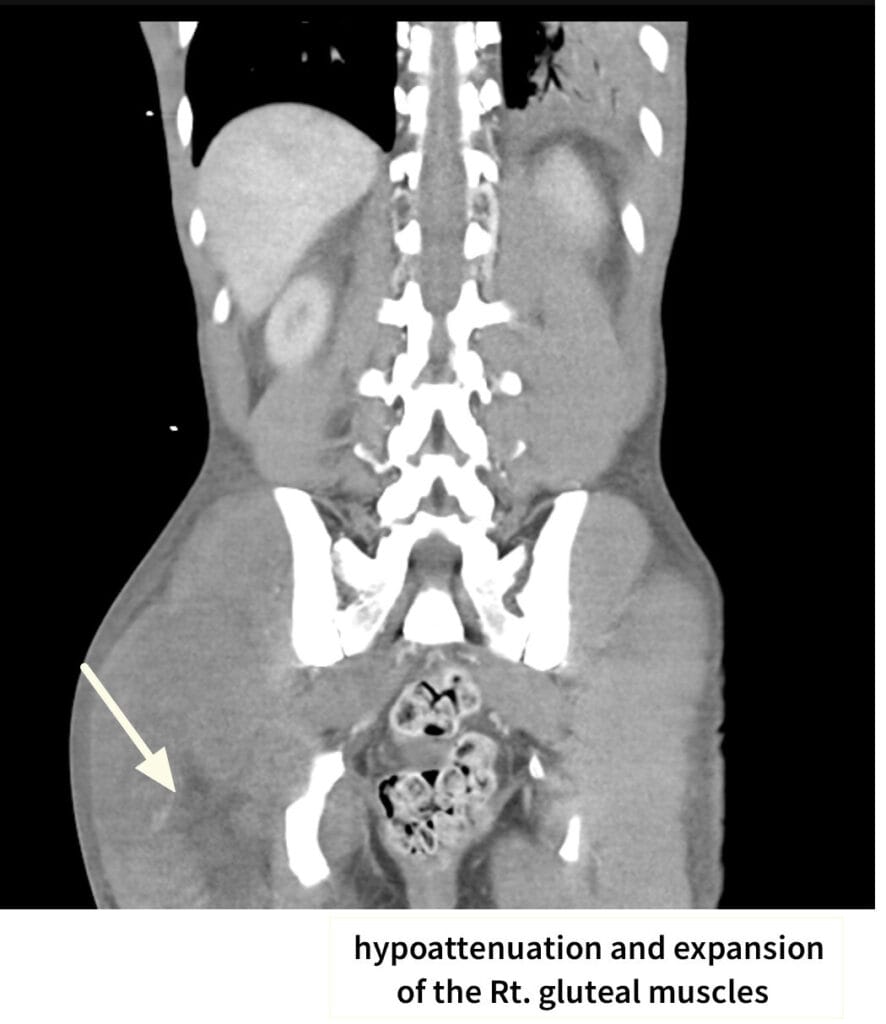
[치료]
– 조기 등장성 결정질 수액으로 충분한 이뇨를 확보합니다(신부전·폐부종 위험은 모니터링하시고 조절합니다).
– 고칼륨혈증은 심전도 감시 하에 표준 알고리즘(칼슘·인슐린/포도당·베타작용
알레르기성 세관·사이질 콩팥염 (Allergic Acute Interstitial Nephritis, AIN)
약물 과민반응 매개 사이질 염증
발열·발진·호산구증가(고전 triad는 드묍니다)
유발 약물 중단 + 필요 시 스테로이드
[정의]
AIN은 주로 약물 과민반응에 의해 세뇨관·사이질에 림프구/호산구 침윤과 부종이 발생하는 염증성 신손상입니다.
[원인/위험요인]
– 항생제(페니실린계, 세팔로스포린, TMP/SMX, 리팜핀), NSAIDs, PPI, 이뇨제 등이 흔한 원인입니다.
– 자가면역/감염 연관 AIN도 드물게 있습니다.
[임상양상]
– 비특이적 피로·구역과 함께 미세혈뇨·백혈구뇨·단백뇨(경도)가 흔합니다.
– 발열·발진·관절통·호산구 증가/호산구뇨가 나타날 수 있으나 모두 동반되지는 않습니다.
[진단]
– 요침사에서 WBC cast·백혈구뇨, 드물게 호산구뇨가 보입니다.
– 확진은 신생검(사이질 염증·부종·호산구 침윤)으로 이루어집니다.
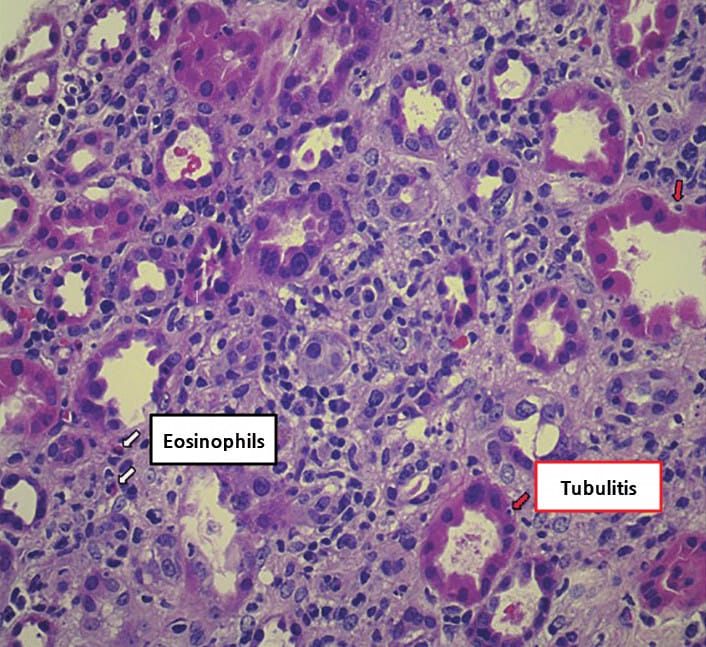

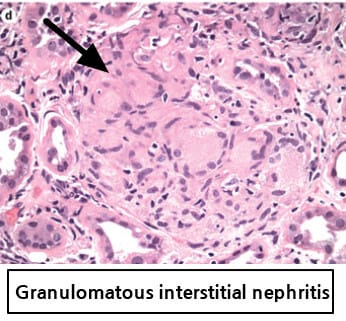
– 약력 확인이 핵심이며, 다른 AKI 원인(ATN/사구체)과 감별합니다.
[치료]
– 유발 약물 즉시 중단이 가장 중요합니다.
– 신기능 회복 지연·중증 시 스테로이드를 고려합니다(예: 전신 스테로이드 단기간, 감량 요법).
– 체액·전해질·산염기 이상을 교정하고, 필요 시 일시적 신대체요법을 시행합니다.
– 재노출을 피하기 위해 약물 알레르기 기록을 명확히 하시는 것이 중요합니다.
사구체·혈관성 원인 (ANCA 혈관염, Anti-GBM 병 등)
빠른 진행 → RPGN 형태로 나타남
혈뇨·단백뇨 + 신기능 급격 악화
조기 면역억제·혈장교환술이 예후 결정
[정의]
사구체·혈관성 원인에 의한 AKI는 자가면역성 염증 반응으로 사구체 모세혈관이 손상되어 급성 신손상이 발생하는 경우입니다.
대개 급속 진행성 사구체신염(RPGN) 형태를 보입니다.
[원인/위험요인]
– ANCA 관련 혈관염: 육아종증(polyangiitis), 현미경적 다발혈관염(MPA), 호산구성 육아종증 혈관염(EGPA)
– Anti-GBM 병: 굿파스처 증후군(폐출혈 + 신부전)
– 전신질환: SLE, 혈전성 미세혈관병증(TMA) 일부도 포함
[임상양상]
– 혈뇨·단백뇨
– 고혈압·부종
– 전신 증상: 발열, 체중 감소, 피부 발진, 폐출혈(특히 Anti-GBM)
– 신기능이 수일~수주 내 급격히 악화됩니다.
[진단]
– 혈액검사: ANCA, Anti-GBM 항체, ANA·dsDNA 등
– 소변: RBC cast, 단백뇨
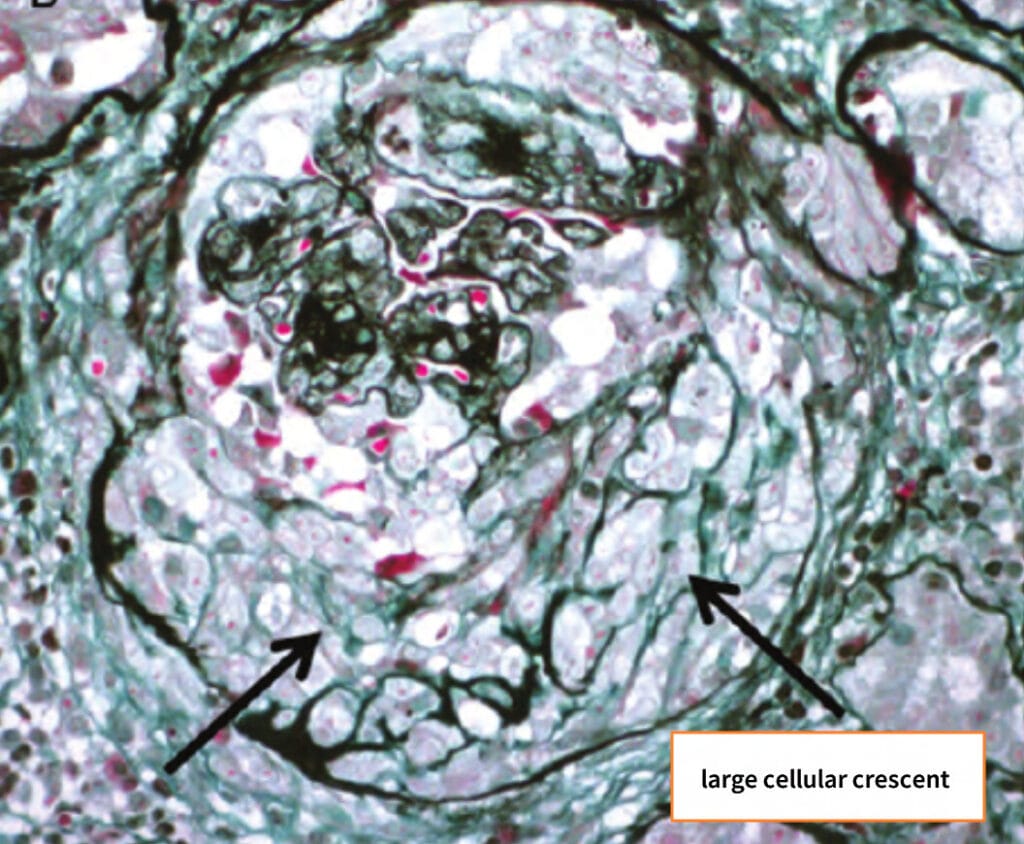
– 신생검: 초승달 모양 병변(crescent) 확인
[치료]
– 스테로이드 + Cyclophosphamide가 표준
– Anti-GBM 병: 혈장교환술(Plasmapheresis) 병행
– 재발·불응성: Rituximab 고려
– 신기능 회복 불가 시 투석/이식 고려
Postrenal AKI
[특징]
신우·요관·방광·요도의 배뇨 경로 폐쇄로 GFR이 감소합니다. (소변이 나오지 못함)

[원인]
– 요관 협착
– 전립선 비대증
– 요로 결석
– 종양(방광암, 전립선암, 자궁경부암)
[임상양상]
배뇨곤란, 빈뇨·절박뇨, 간헐적 무뇨/다뇨가 반복될 수 있고,
– 신장·방광 초음파에서 수신증이 보입니다.
[치료]
– 즉시 감압 배액(Foley 카테터)으로 신손상을 멈춤.
if ) 상부 폐쇄면 요관 스텐트 또는 경피적 신루(nephrostomy)를 시행합니다.
– BPH에는 알파차단제(탐스로신)·5α 환원효소 억제제를 고려하고,
– 재발성 폐쇄에는 수술(TURP 등)을 검토합니다.
*감압 후 후이뇨(post-obstructive diuresis)가 올 수 있움
> 전해질·체액 균형을 면밀히 교정해야 함.
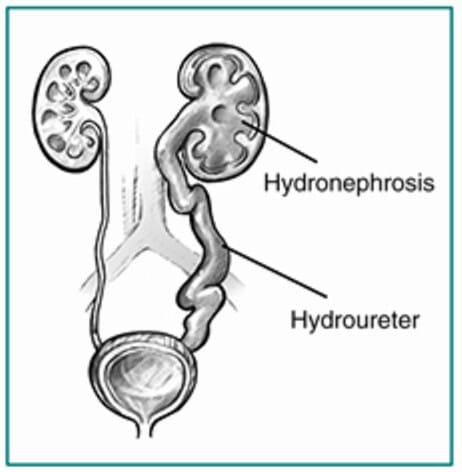
수신증 (Hydronephrosis, Post-renal Obstruction)
배뇨 경로 폐쇄 → 사구체여과 저하
초음파 수신증 확인 → 신속한 감압이 핵심
감압 후 후이뇨·전해질 교정이 필요합니다
[정의]
수신증은 요로 폐쇄로 신우·신배가 확장되는 상태이며, 양측 또는 단일 기능 신장의 일측 폐쇄는 급성 신손상의 중요한 원인입니다.
[원인/위험요인]
– 상부: 요관 결석·협착·종양·혈전·섬유화가 흔합니다.
– 하부: BPH·전립선암·요도협착·신경인성 방광·혈전/결석으로 인한 방광출구 폐색입니다.
– 임신·수술/방사선 후 변화·결핵성 요관협착도 원인이 됩니다.
[임상양상]
– 옆구리 산통·배뇨곤란·간헐적 무뇨/소량뇨가 나타납니다.
– 감염 동반 시 발열·오한·패혈증 위험이 있습니다.
[진단]
– 1차: 신장/방광 초음파에서 수신증과 잔뇨를 확인합니다.
– CT(비조영 또는 조영)로 폐쇄 위치·원인을 파악하고, 요분석·크레아티닌·전해질을 평가합니다.
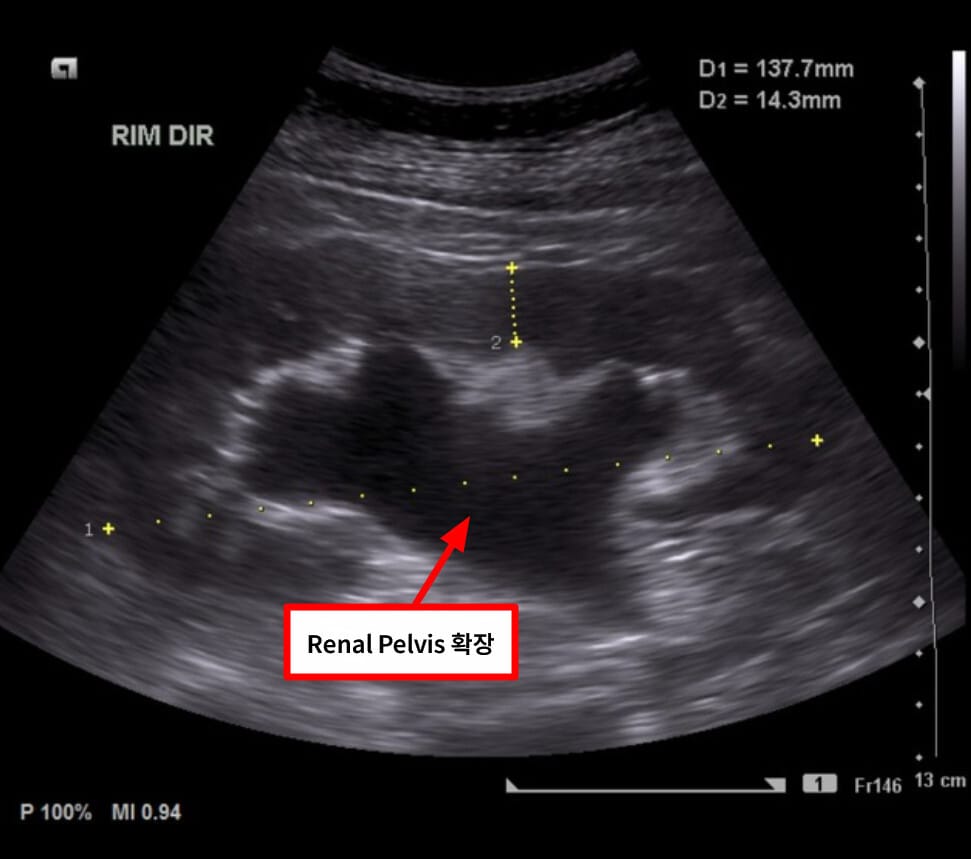

Qaqish N, Hydronephrosis. Case study, Radiopaedia.org (Accessed on 14 May 2025) https://doi.org/10.53347/rID-76671

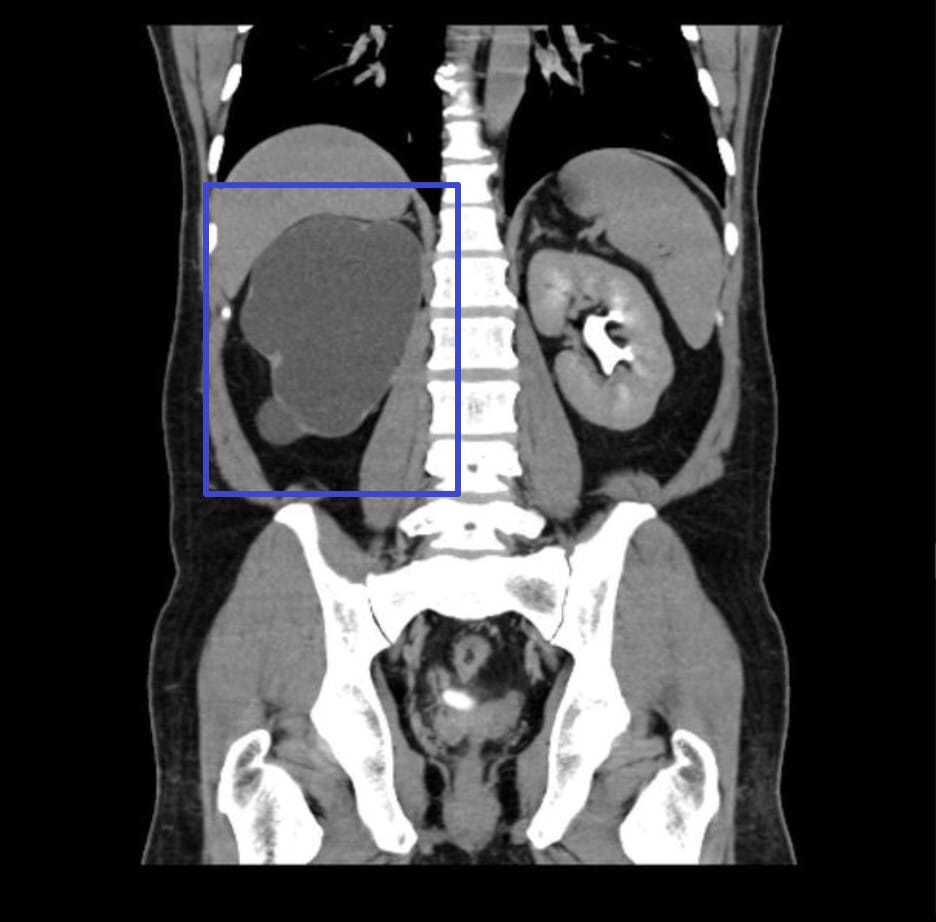
Bhattarai A, Gross hydronephrosis. Case study, Radiopaedia.org (Accessed on 14 May 2025) https://doi.org/10.53347/rID-93278
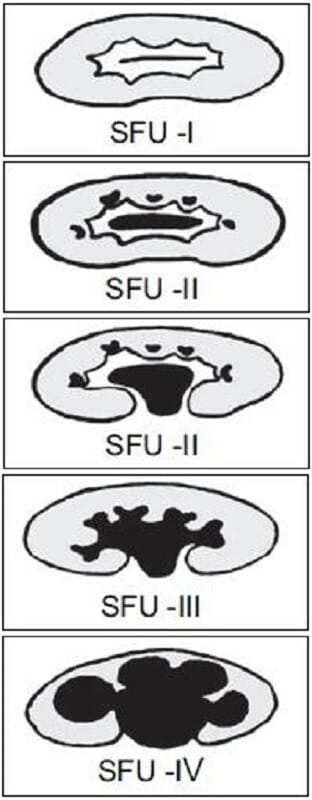
[치료]
– 즉시 감압이 최우선입니다: 하부 폐색은 Foley 유치, 상부 폐색은 요관 스텐트 또는 경피적 신루를 시행합니다.
– 감염 동반 폐쇄는 항생제와 동시 감압이 필수입니다.
– 원인 교정: BPH는 α1-차단제 ± 5ARI 후 TURP/HoLEP 고려, 결석은 ESWL/URS/PCNL를 선택합니다.
– 감압 후 후이뇨가 발생할 수 있어 수액·전해질 균형을 엄밀히 교정합니다.
만성 신부전
만성 신질환 (Chronic Kidney Disease, CKD)
3개월 이상 지속되는 eGFR 감소 또는 신손상 소견
가장 흔한 원인은 당뇨병성 신증과 고혈압성 신증
RAAS 억제제·SGLT2 억제제로 진행 억제
[정의]
CKD는 3개월 이상 사구체여과율이 60 미만이거나, 단백뇨·영상학적 이상 등 신손상 증거가 지속될 때 진단됩니다. 진행하면 말기 신부전(ESKD)으로 투석 또는 이식이 필요합니다.
[원인/위험요인]
– m/c: 당뇨병성 신증
– 그 다음: 고혈압성 신증
– 기타: 사구체신염, 다낭성 신질환, 역류성 신병증, 약물성 신손상
– 위험요인: 흡연, 비만, 반복된 AKI, 가족력
[임상양상]
– 초기: 무증상, 혈액검사에서만 발견되는 경우 많음
-> 진행 시: 부종, 피로, 야뇨
-> 말기:
– 요독증(소양감, 구토, 인지저하)
– 빈혈(EPO 결핍)
– 골대사 이상(저칼슘혈증, 2차성 부갑상선항진증)
– 고칼륨혈증
[진단]
– 혈액검사: eGFR(CKD-EPI), 전해질
– 소변검사: 단백뇨, UACR(알부민/크레아티닌 비율)
– 영상: 초음파에서 신장 크기 감소
– 원인 불명 시: 신생검
[치료]
치료의 목표는 질환 진행 억제와 합병증 관리입니다.
– 생활습관: 저염식, 단백질 적정 섭취(0.6~0.8 g/kg/d), 금연, 체중조절
– 약물치료: ·
> ACEi/ARB: 단백뇨 억제
> SGLT2 억제제: eGFR 보존
> 이뇨제: 부종 조절
> 인결합제·비타민 D: 골대사 이상 교정
> ESA: 빈혈 교정
– 신대체요법: 투석(혈액투석/복막투석) 또는 신장이식
당뇨병성 신증 (Diabetic Nephropathy)
[특징]
– 미세알부민뇨에서 거대알부민뇨로 진행
– 망막병증 동반이 흔하고 사구체 기저막 비후·Kimmelstiel–Wilson 결절 소견
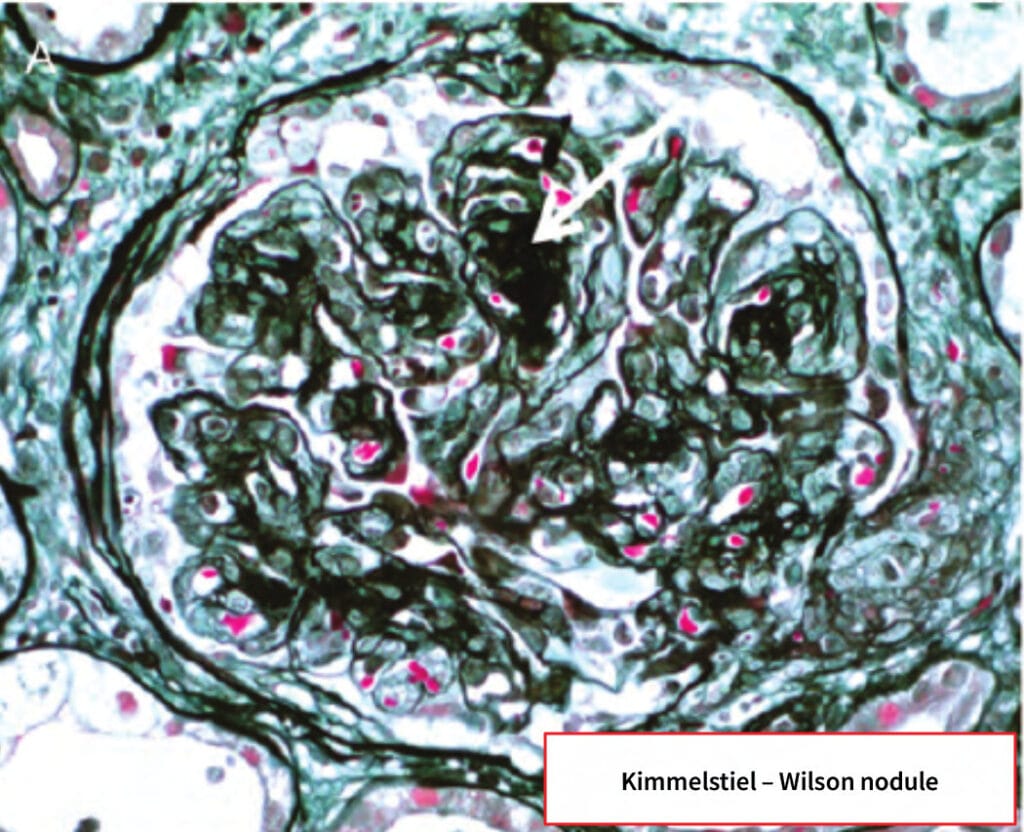
– 조기에는 과여과로 eGFR이 높다가 -> 점진적 감소로 전환됩니다.
[임상양상]
– 무증상 알부민뇨로 시작하며, 진행 시 부종·야뇨·고혈압이 두드러집니다.
– 말기에는 요독 증상과 빈혈·골대사 이상이 동반됩니다.
[치료]
– 혈당 조절(HbA1c 약 7% 전후, 저혈당 위험 고려) , 혈압 조절 <130/80
a) 알부민뇨가 있으면
: ACEi/ARB로 단백뇨를 감소시키고,
eGFR 20 이상에서는 SGLT2 억제제를 병용하여 진행과 심혈관 사건을 억제합니다.
b) 잔여 단백뇨가 지속되면
: Finerenone(비스테로이드성 MRA)을 고려하고,
지질관리(스타틴)·체중감량·흡연중단을 병행합니다.
– GLP-1 RA는 심혈관 보호와 체중감량에 유익할 수 있습니다.
고혈압성 신증 (Hypertensive Nephrosclerosis)
[특징]
– 장기간의 고혈압으로 소혈관 hyaline arteriolosclerosis가 진행하며, 양측 신장이 작아지고 표면이 과립화됩니다.
– 악성 고혈압에서는 망막 출혈/유두부종, 미세혈관 용혈, 급속한 신기능 악화가 동반될 수 있습니다.
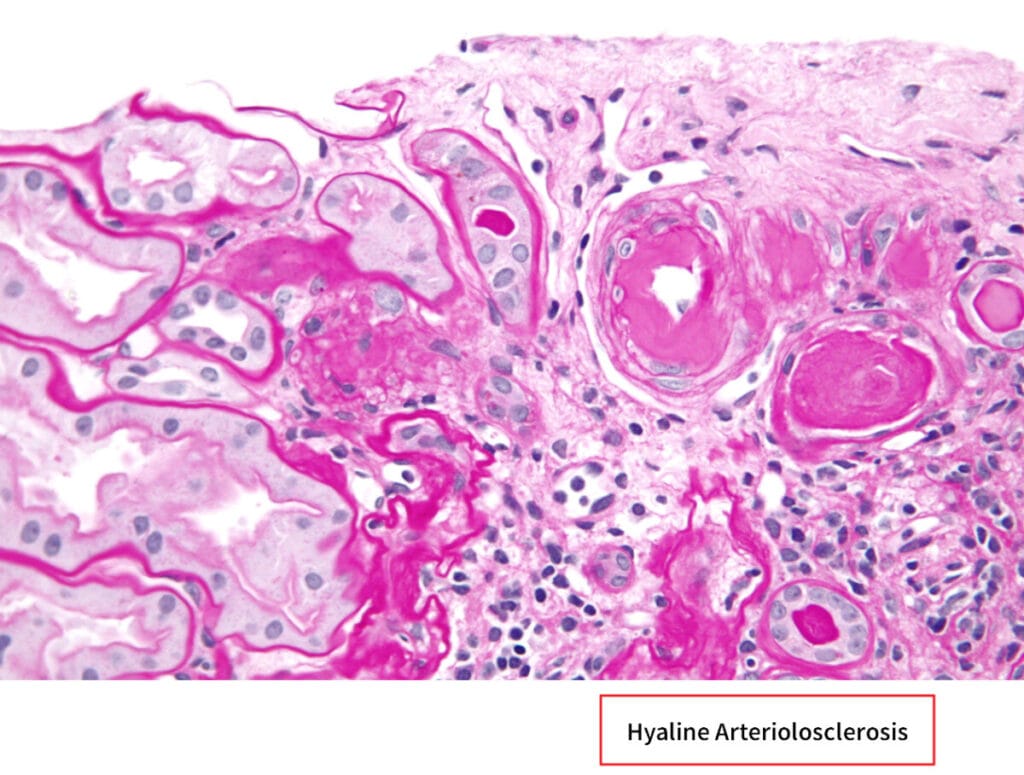
[임상양상]
– 서서히 진행하는 미세알부민뇨·신기능 저하와 함께 난치성 고혈압이 동반될 수 있습니다.
– 말기에 야뇨·피로·부종이 두드러집니다.
[치료]
– 엄격한 혈압 조절이 가장 중요하며, 단백뇨가 있으면 ACEi/ARB를 우선 사용합니다.
– 이뇨제(Thiazide, Loop diuretics), 칼슘채널차단제(DHP 우선) 등을 병합하고, 염분 섭취를 제한합니다.
– 악성 고혈압은 입원하여 정주 항고혈압제로 단계적 혈압 하강을 시행합니다.
사구체질환 관련 CKD
[특징]
IgA 신병증, FSGS, 막성 신증 등에서 지속적 단백뇨·혈뇨와 점진적 eGFR 감소가 나타납니다.
면역매개 염증과 섬유화가 병태의 핵심입니다.
[임상양상]
거품뇨·현미경적 혈뇨, 부종·고혈압이 흔하고, 재발성 육안적 혈뇨가 병력을 시사할 수 있습니다.
[치료]
– 단백뇨 표적 치료(ACEi/ARB, SGLT2 억제제)와 혈압 조절.
– 질환별로 스테로이드·칼시뉴린 억제제·리툭시맙 등 면역치료를 선택하며,
if) 재발·고위험군: 신생검 결과에 따라 맞춤 치료합니다.
다낭성 신질환 (Polycystic Kidney Disease)
[특징]
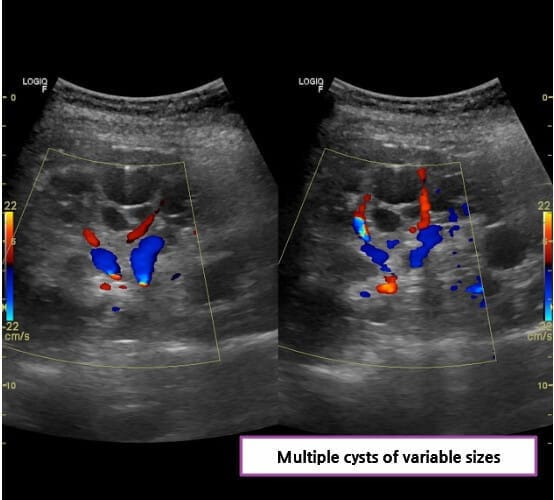
양측 신장에 다수의 낭종으로 신장이 비대해지고, 조기 고혈압과 통증·혈뇨·감염이 잦습니다.
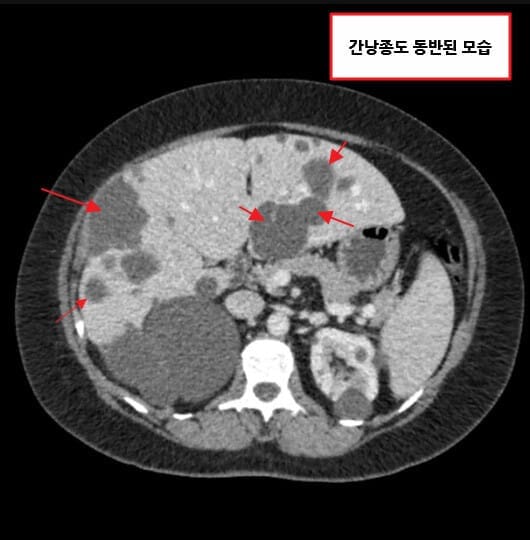
간낭종, 두개강내 동맥류, 판막질환 등 신외 합병증이 동반될 수 있습니다.
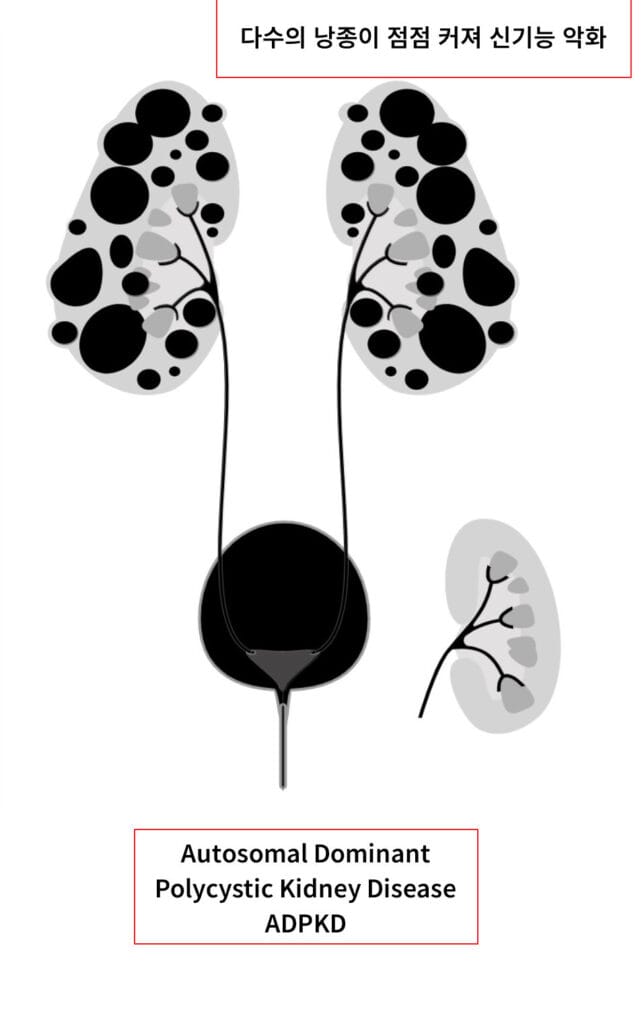
[임상양상]
옆구리 통증(낭종 팽창/출혈), 육안적 혈뇨, 재발성 상부 UTI·낭종 감염, 신장결석(요산/칼슘) 등이 흔합니다.
가족력이 단서가 되며, 신장 초음파에서 다발성 낭종이 확인됩니다.
[치료]
혈압 조절과 염분 제한, 충분한 수분섭취를 권고합니다.
– 진행 위험이 높으면 Tolvaptan을 고려하며 간기능 모니터링이 필요합니다.
– 낭종 감염은 지용성 항생제(Fluoroquinolone, Bactrim 등) 를 통해 치료
– 고위험군에서는 뇌동맥류 선별을 고려하고, 말기에는 투석/이식을 시행합니다.
기타 원인
[특징/임상]
역류성 신병증(반복성 UTI·상흔으로 인한 신축소), 약물성 신병증(진통제 신증), 장기 폐쇄성 요로병증 등 다양한 경로로 CKD가 발생합니다.
[치료]
원인 차단이 최우선이며, 요로폐쇄 해소·감염 예방·약물 중단과 함께 CKD 표준 치료(혈압·단백뇨·지질·생활습관 교정)를 병행합니다.
사구체 질환
신증후군 (Nephrotic Syndrome)
단백뇨 > 3.5 g/일
저알부민혈증 + 부종 + 고지질혈증
감염과 혈전증 위험 증가
[정의]
신증후군은 대량의 단백뇨로 인해 저알부민혈증, 전신 부종, 고지질혈증이 동반되는 임상 증후군입니다.혈장 단백이 소변으로 빠져나가면서 삼투압이 낮아지고, 부종이 전신에 나타나게 됩니다.

[원인/위험요인]
– 원발성: 소아에서 흔한 Minimal Change Disease, 성인에서는 FSGS, 막성사구체신염(MGN)
– 이차성: 당뇨병성 신증, 루푸스, B형·C형 간염, 악성종양, 약물(NSAIDs)
[임상양상]
– 전신 부종: 안검부종에서 시작해 말초·복수로 진행
– 거품뇨: 단백 소실로 인한 대표적 소견
– 혈전 경향: 특히 막성신증에서 흔함
– 감염 위험 증가: 면역글로불린, 보체 단백의 소실 때문
[진단]
– 요검사: 24시간 단백뇨 정량(>3.5 g/일)
– 혈액검사: 저알부민혈증, 고지질혈증
– 요침사: 무형성 원주(특징적)
– 성인 대부분은 신생검 필요 (원인 질환 확인)
[치료]
치료의 목표는 부종과 단백뇨 조절, 합병증 예방입니다.
– 생활습관: 저염식, 수분 조절, 감염 예방(예방접종 권장)
– 약물치료:
· 이뇨제: 부종 조절
· ACEi/ARB: 단백뇨 감소
· 스타틴: 고지질혈증 교정
· 면역억제제: 스테로이드(MCD), 칼시뉴린 억제제, 리툭시맙 등
– 고위험군에서는 항응고제 고려
Minimal Change Disease (MCD)
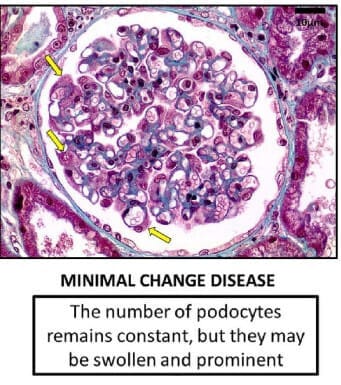
Minimal Change Disease (최소변화병증)
T세포 이상으로 인해 podocyte의 구조적 손상이 발생하며, 단백질 여과 장애가 생깁니다.
[특징]
소아에서 가장 흔한 신증후군 원인입니다.
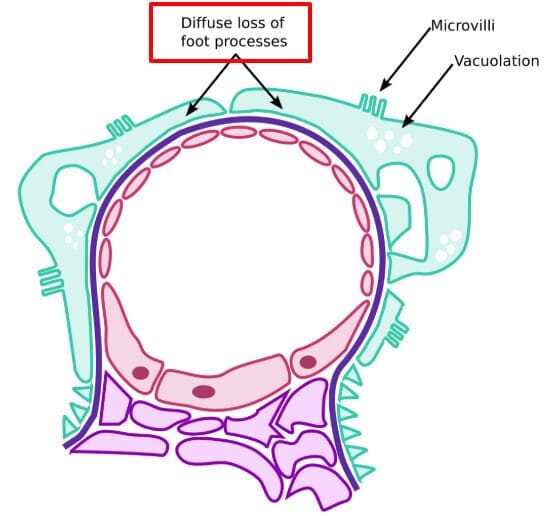
광학현미경에서는 정상으로 보이지만, 전자현미경에서 podocyte의 foot process 소실/ 광범위한 유합이 관찰됩니다.
[치료]
스테로이드에 반응이 매우 좋은 것이 특징입니다.
Focal Segmental Glomerulosclerosis (FSGS)
Podocyte 손상 및 사구체 내압 증가로 일부 사구체가 국소적으로 경화
[특징]
성인에서 흔한 원인입니다.
사구체 일부 분절(segmental) 부위에서 경화가 나타납니다.
예후는 불량하며, 종종 신부전으로 진행합니다.
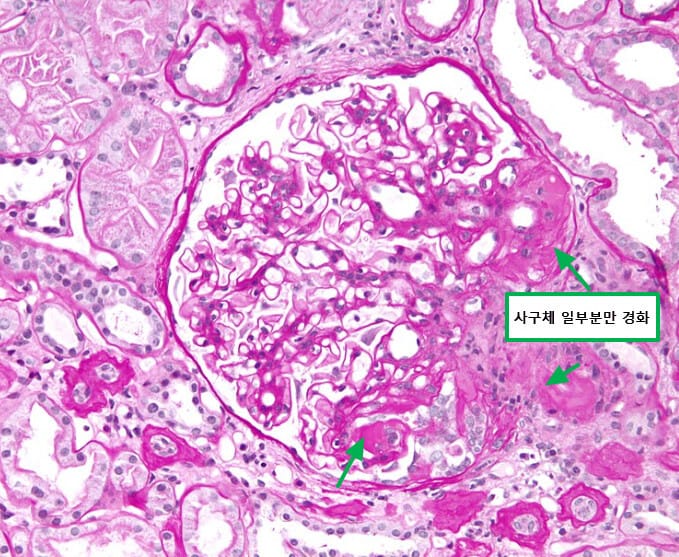
→ 일부 사구체(focal),에서, 일부 부위만(segmental) 경화 및 손상된 것이 특징입니다.
[치료]
스테로이드, 칼시뉴린 억제제, RAAS 억제제를 사용합니다.
막성 사구체신염 (Membranous GN)
자가항체(PLA2R 등)에 의해 기저막 외측에 면역복합체가 침착되어 손상이 유발됩니다.
[특징]
성인 신증후군의 주요 원인입니다.
자가항체(anti-PLA2R)와 관련이 있으며, 모세혈관벽이 두꺼워집니다.

→ 위 그림에서 검은색으로 염색된것이 기저막 (Basement membrane)입니다. 사구체 기저막이 비후되고, 면역복합체가 기저막 외측에 침착되어 스파이크 형성이 나타납니다.
[임상]
심한 단백뇨와 부종이 나타나고,
혈전증 위험이 높은 것이 특징입니다.
[치료]
RAAS 억제제, 면역억제제(스테로이드, 칼시뉴린 억제제, 리툭시맙)를 사용합니다.
막증식성 사구체신염 (Membranoproliferative Glomerulonephritis, MPGN)
– 사구체 기저막 비후와 이중 윤곽(double contour) 형성이 병리학적 특징
– 보체 경로 이상과 면역복합체 침착
– 신증후군과 신염증후군이 혼재된 양상을 보이는 대표적 질환
[정의]
– MPGN은 사구체 기저막과 Mesangium에 면역복합체 또는 보체 관련 단백이 침착되어 발생하는 만성 사구체질환입니다.
– 광학현미경에서는 사구체 기저막 이중화와 Mesangium 증식이 특징적으로 관찰됩니다.

[원인/위험요인]
– 가장 흔한 원인은 만성 감염(특히 HCV, HBV)과 면역복합체 형성입니다.
– 자가면역질환(SLE 등), 단백혈증(예: 다발성 골수종)과 관련되기도 합니다.
– 보체 대체경로 조절 이상(C3 nephritic factor, 보체 조절 단백 결함)도 주요 위험인자입니다.
[임상양상]
– 단백뇨와 혈뇨가 함께 나타나는 신증후군+신염증후군 혼합 양상이 흔합니다.
– 부종, 고혈압이 동반될 수 있으며, 일부 환자는 점진적으로 신부전으로 진행합니다.
– 혈뇨는 현미경적 혈뇨부터 육안적 혈뇨까지 다양하게 나타납니다.
[진단]
– 소변검사: 단백뇨와 혈뇨 동반 확인
– 혈액검사: C3 보체 감소가 흔히 관찰됨
– 신장생검: 광학현미경에서 사구체 기저막의 이중 윤곽(double contour), 전자현미경에서Immune deposits 확인
– 면역형광검사: IgG, C3 침착이 흔히 관찰됨
[치료]
– 치료의 목표는 단백뇨 감소와 신기능 보존입니다.
– 생활습관: 염분 제한, 혈압 조절
– 약물치료: ACE 억제제/ARB를 통한 단백뇨 감소 및 혈압 조절
– 면역억제제: 스테로이드, 사이클로포스파미드, 리툭시맙 등이 선택적으로 사용됨
– 원인 교정: HCV/HBV 감염 시 항바이러스 치료, 기저 질환 치료
– 말기 신부전으로 진행 시 투석이나 신이식이 필요할 수 있습니다.
이차성 신증후군
[원인]
당뇨병성 신증(Diabetic nephropathy)
- 가장 흔한 원인
- 고혈당으로 인한 사구체 기저막 손상
전신홍반루푸스(SLE, Systemic Lupus Erythematosus)
- 자가면역질환에 의한 사구체 손상
감염 (Infection)
- B형·C형 간염, HIV, 말라리아, 매독 등
약물 (Drugs)
- 페니실라민, NSAIDs, 인터페론 등
종양 (Malignancy)
- 림프종(특히 Hodgkin lymphoma)
- 고형암(폐암, 위암 등)
기타 전신질환
- 다발성 골수종(Multiple myeloma)
- 아밀로이드증(Amyloidosis)
[치료]
원인 질환 조절이 가장 중요합니다.
병행하여 단백뇨 감소를 위한 RAAS 억제제와 이뇨제 등을 사용합니다.
신염증후군 (Nephritic Syndrome)
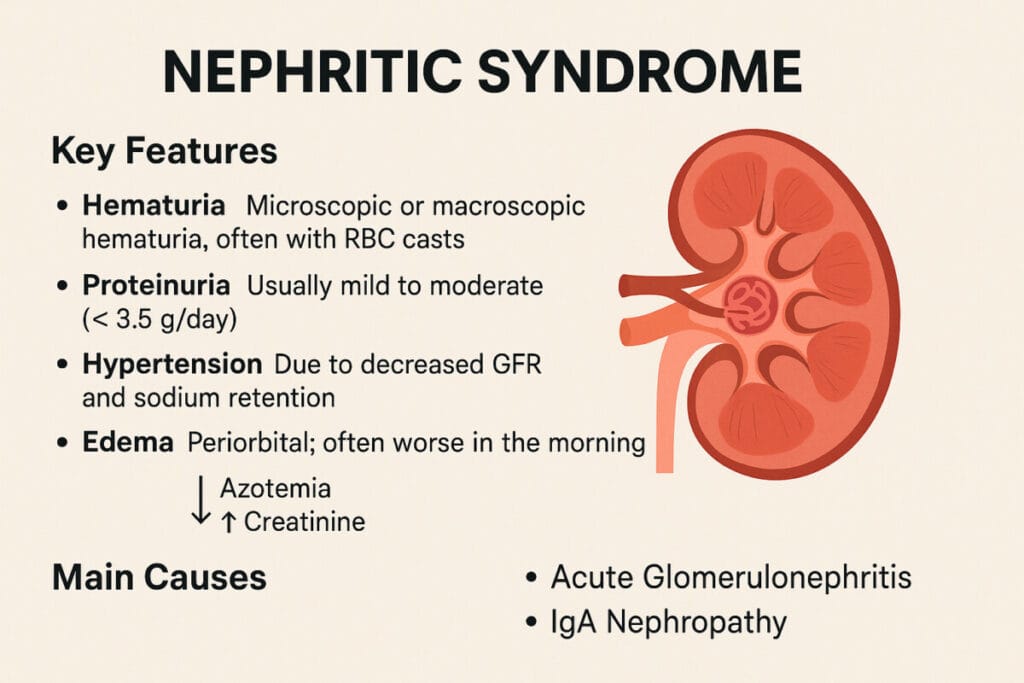
혈뇨(RBC 원주) + 단백뇨(중등도)
고혈압과 부종 동반
사구체 염증
[정의]
신염증후군은 혈뇨와 단백뇨를 특징으로 하며,
사구체의 염증으로 인해 여과 기능이 떨어지고 전신적 증상이 나타나는 임상 증후군입니다
[원인/위험요인]
– 대표적 원인: 급성 사구체신염(Post-streptococcal GN)
– 기타: IgA 신병증, 루푸스 신염, ANCA 관련 혈관염
– 위험요인: 선행 감염(특히 연쇄상구균), 자가면역질환
[임상양상]
– 혈뇨: 현미경적 또는 육안적 혈뇨 (콜라색 소변)
– 단백뇨: 보통 3.5 g/일 미만
– 부종: 안면·하지 중심
– 고혈압: 신장의 염증과 체액 저류로 인해 발생
[진단]
– 소변검사: 혈뇨, 단백뇨, RBC 원주
– 혈액검사: 보체 감소(C3), 항체검사(ASO, ANA, ANCA)
– 영상: 신장 초음파 (신장 크기·폐쇄 여부 확인)
– 원인 불명 시: 신생검
[치료]
치료의 목표는 원인 질환 조절과 합병증 예방입니다.
– 생활습관: 저염식, 수분 조절
– 약물치료:
· 고혈압 조절(ACEi/ARB, 이뇨제)
· 면역억제제(루푸스, ANCA 혈관염 등에서 스테로이드·사이클로포스파미드)
– 감염 후 GN은 대체로 지지적 치료 (대부분 자연 회복)
– 심한 경우: 투석
연쇄상구균 감염 후 사구체신염 (Acute Post-streptococcal GN)
연쇄상구균 감염(인두염, 피부감염) 후 약 1~3주 뒤 발생합니다.
Triad – 혈뇨, 부종, 고혈압
[정의]
– 급성 사구체신염은 A군 β-용혈성 연쇄상구균 감염(인두염, 농가진 등) 이후 발생하는 면역복합체 매개성 사구체질환입니다.
– 항체와 세균항원이 결합해 면역복합체를 형성하고, 이것이 사구체에 침착되어 보체 활성화와 염증을 유발합니다.
[원인/위험요인]
– 가장 흔한 원인은 A군 사슬알균 감염입니다.
– 위험요인으로는 소아(특히 5~12세), 피부 감염(농가진) 또는 인두염 병력, 위생 환경이 열악한 경우가 있습니다.
[임상양상]
– 혈뇨: 콜라색/적갈색 소변 (적혈구 원주 동반)
– 단백뇨: 보통 경도~중등도
– 부종: 주로 안면, 특히 아침에 심함
– 고혈압: 체액 저류와 사구체 기능 저하로 발생
– 전신 증상: 피로, 식욕 부진, 소변량 감소
[진단]
혈액검사에서 ASO 상승, 보체(C3) 감소가 특징적입니다.
– 기본검사: 소변검사(혈뇨, 단백뇨, 적혈구 원주), 혈액검사(크레아티닌 상승, BUN 증가)
– 특수검사: 항스트렙톨리신 O (ASO) 상승, C3 보체 감소
– 조직검사(필요 시): 광학현미경에서 확산성 사구체 증식, 면역형광검사에서 granular C3 침착 확인
[치료]
– 치료의 목표는 합병증 예방과 보존적 신기능 유지입니다.
– 생활요법: 나트륨 및 수분 제한, 혈압 조절
– 약물치료: 이뇨제(부종, 고혈압 조절), 항고혈압제(ACE 억제제/ARB)
– 항생제: 잔존한 사슬알균 감염 시 페니실린 투여
– 중증(급성 신부전, 뇌증, 심한 고혈압) 시 투석 필요할 수 있음
IgA 신병증 (IgA Nephropathy, Berger’s Disease)
– 가장 흔한 원발성 사구체신염
– 상기도 감염 직후 혈뇨가 특징 (“synpharyngitic hematuria”)
– 사구체에 IgA 면역복합체 침착
[정의]
– IgA 신병증은 사구체에 IgA 면역복합체가 침착하여 발생하는 만성 면역매개성 사구체신염입니다.
– 세계적으로 가장 흔한 원발성 사구체질환이며, 발병 기전은 비정상적인 IgA1 생성 및 제거 장애와 관련됩니다.
[원인/위험요인]
– 가장 흔한 원인은 비정상적 IgA1의 과생산과 사구체 침착입니다.
– 위험요인으로는 상기도 감염(인두염, 편도염), 젊은 남성(특히 15~35세), 아시아 인종, 가족력(유전적 소인)이 있습니다.
[임상양상]
– 육안적 혈뇨: 감염 직후 발생하는 것이 특징적
– 현미경적 혈뇨: 무증상으로 발견되기도 함
– 단백뇨: 경도에서 중등도까지, 신증후군 범위로 진행 가능
– 고혈압: 신손상이 진행되면서 발생
– 일부 환자는 만성 신부전으로 진행
[진단]
– 기본검사: 소변검사(혈뇨, 단백뇨), 혈액검사(혈청 크레아티닌, eGFR)
– 면역검사: 혈청 IgA 상승 가능
– 확진: 신장 생검에서 면역형광검사 시 사구체 메산지움에 IgA 침착 확인
– 영상검사는 특이적 소견은 없으며 배제 목적
[치료]
– 치료의 목표는 단백뇨 감소와 신장 기능 보존입니다.
– 생활습관: 저염식, 혈압 관리
– 약물치료: ACE 억제제/ARB로 단백뇨와 혈압 조절
– 면역억제제: 스테로이드 ± 면역억제제(중등도~중증 단백뇨 시)
– 진행성 신부전 시 투석이나 신이식 고려
루푸스 신염 (Lupus Nephritis)
– 전신홍반루푸스(SLE)의 가장 심각한 장기 침범 중 하나
– 단백뇨와 혈뇨가 대표적 소견
– WHO/ISN 분류에 따라 병리학적 아형 결정
[정의]
– 루푸스 신염은 자가면역질환인 전신홍반루푸스(SLE)가 신장을 침범하여 발생하는 면역복합체성 사구체신염입니다.
– 항-dsDNA 항체 등 자가항체와 면역복합체가 사구체에 침착하면서 보체 활성화와 염증을 일으켜 신장 기능 손상을 초래합니다.
[원인/위험요인]
– 가장 흔한 원인은 SLE에 의한 면역복합체 침착입니다.
– 위험요인으로는 고역가 항-dsDNA 항체, 낮은 보체 수치(C3, C4), 아시아 및 아프리카계 인종, 여성, 조기 발병 SLE 환자 등이 있습니다.
[임상양상]
– 단백뇨: 사구체 손상으로 단백이 소변으로 유출됨
– 혈뇨: 현미경적 또는 육안적 혈뇨 발생
– 부종: 저알부민혈증 및 나트륨 저류로 인한 부종
– 고혈압: 신기능 저하와 나트륨·수분 저류로 발생
– 진행 시 신부전까지 이어질 수 있음
[진단]
– 기본검사: 소변 검사(단백뇨, 혈뇨), 혈액검사(혈청 크레아티닌, 보체 수치, 항-dsDNA 항체)
– 특수검사: 신장 생검이 가장 중요한 확진법으로, 병리학적 WHO/ISN 분류(I~VI형) 결정
– 영상검사: 신장 크기와 구조 확인용, 그러나 특이도는 낮음
[치료]
– 치료의 목표는 신장 기능 보존과 단백뇨 억제입니다.
– 생활습관: 나트륨 제한, 혈압 조절, 금연 권장
– 약물치료: 글루코코르티코이드 + 면역억제제(Cyclophosphamide, Mycophenolate mofetil) 병용
– 고혈압 동반 시 ACE 억제제/ARB 투여하여 단백뇨 감소
– 불응성의 경우 Rituximab 같은 생물학적 제제 고려
ANCA 연관 혈관염 (ANCA-associated Vasculitis, AAV)
– 소혈관을 침범하는 전신성 혈관염
– 대표적으로 GPA, MPA, EGPA 세 가지 아형
– ANCA 항체가 중요한 진단 및 병리 기전
[정의]
– ANCA 연관 혈관염은 항호중구세포질항체(ANCA)에 의해 유발되는 자가면역성 소혈관염입니다.
– 호중구가 활성화되어 혈관 내피를 손상시키며, 주로 신장, 폐, 상기도 등 다양한 장기를 침범합니다.
– 대표 아형은 다발혈관육아종(GPA), 현미경다발혈관염(MPA), 호산구성 다발혈관염(EGPA)입니다.
[원인/위험요인]
– 가장 흔한 원인은 ANCA (c-ANCA: PR3, p-ANCA: MPO)에 의한 호중구 활성화입니다.
– 위험요인으로는 유전적 소인(HLA 연관성), 감염, 약물(프로필티오우라실 등), 환경적 노출(실리카, 흡연)이 제시됩니다.
[임상양상]
– 신장 침범: 혈뇨, 단백뇨, 신부전 (신속 진행성 사구체신염)
– 폐 침범: 폐출혈, 결절성 병변, 호흡곤란
– 상기도 침범(GPA): 만성 부비동염, 비중격 천공
– 말초 신경계 침범(EGPA): 다발신경병증
– 전신 증상: 발열, 체중 감소, 피로, 관절통
[진단]
– 기본검사: 소변검사(혈뇨, 단백뇨), 혈액검사(염증수치, 크레아티닌)
– 면역검사: ANCA 검사 (c-ANCA: PR3, p-ANCA: MPO)가 핵심
– 영상검사: 흉부 CT에서 폐결절, 출혈, 섬유화 소견
– 조직검사: 신장·폐 생검에서 괴사성 혈관염 및 초승달 형성 사구체신염 확인
[치료]
– 치료의 목표는 질병 활성 억제와 장기 손상 방지입니다.
– 급성기: 고용량 글루코코르티코이드 + Cyclophosphamide 또는 Rituximab
– 유지치료: Azathioprine, Methotrexate, Mycophenolate mofetil
– 신부전 또는 폐출혈 심한 경우 혈장교환술 고려
– 고혈압/단백뇨 조절을 위해 ACE 억제제/ARB 병용 가능
낭성 신질환
다낭성 신질환 (Polycystic Kidney Disease, PKD)
양측 신장에 다수의 낭종
조기 고혈압 및 신기능 저하
간낭종, 뇌동맥류 등 신외 합병증 동반
[정의]
다낭성 신질환은 유전적 이상으로 인해 신실질에 다수의 낭종이 발생하여 점차 커지고, 결국 신장이 비대해지면서 만성 신부전으로 진행하는 질환입니다.
[원인/위험요인]
– ADPKD: PKD1, PKD2 유전자 변이
– ARPKD: PKHD1 유전자 변이
– 가족력, 남성, 조기 고혈압, 반복 혈뇨가 진행 위험을 높입니다.
[임상양상]
– 옆구리 통증과 혈뇨가 흔히 나타납니다.
– 조기에 고혈압이 발생하며, 재발성 요로감염과 신장결석이 동반될 수 있습니다.
– 간낭종, 뇌동맥류 파열 등 신외 합병증이 발생할 수 있습니다.
[진단]
– 신장 초음파에서 다수의 낭종을 확인하여 진단합니다.
– CT/MRI에서 낭종의 분포와 크기를 정밀하게 평가하며, 총신장용적(TKV)을 측정하여 예후를 예측합니다.
– 필요 시 유전자 검사를 통해 확진할 수 있습니다.


[치료]
– 혈압 조절(ACEi/ARB)과 염분 제한이 중요합니다.
– 진행 위험군에서는 Tolvaptan을 고려할 수 있으며, 간기능을 정기적으로 확인해야 합니다. (간낭종 포함 )
– 낭종 감염 시 지용성 항생제를 사용합니다.
– 말기에는 투석 또는 신장이식이 필요합니다.
신혈관 질환
신동맥 협착 (Renal Artery Stenosis, RAS)
[정의]
신동맥 내경이 유의하게 좁아져 신장 관류가 감소하고, 레닌-안지오텐신-알도스테론 시스템 (RAAS)이 활성화되어 고혈압과 신기능 저하를 유발하는 상태를 말합니다.

[원인/위험요인]
– 가장 흔한 원인은 죽상경화증이며 고령, 흡연, 당뇨, 고지혈증이 위험을 높입니다.
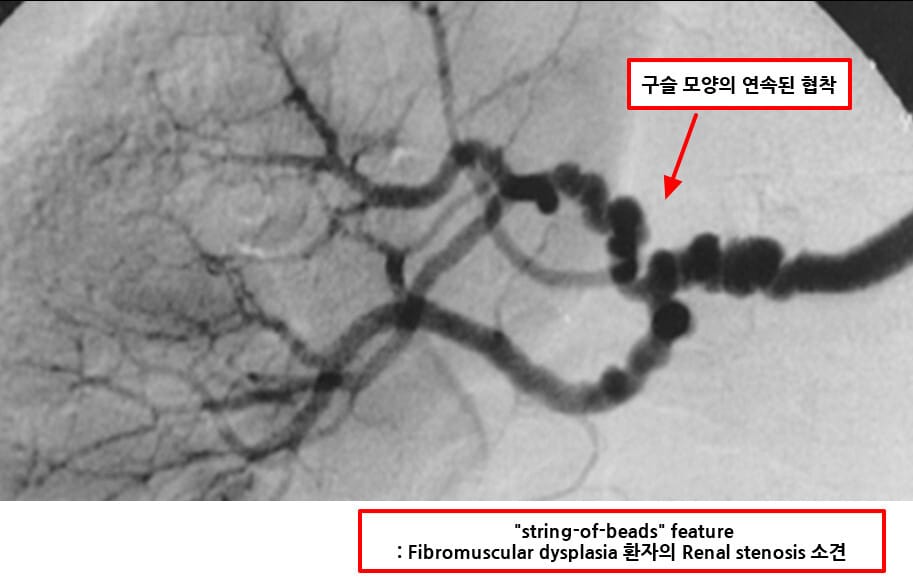
– 젊은 여성에서는 섬유근형성이상(FMD)이 원인이 될 수 있습니다.
[임상양상]
– 치료에 잘 반응하지 않는 고혈압 (약물 난치성 고혈압)
– 신부전: 양측성 협착 또는 단일 신장 협착 시 더 심함
– 청진 시 복부 잡음
– ACE 억제제/ARB 투여 후 급격한 크레아티닌 상승이 특징적
– 부종, 단백뇨 동반 가능
[진단]
– 기본검사: 혈액검사(크레아티닌, eGFR), 소변검사(단백뇨)
– 영상검사: 신동맥 도플러 초음파 (비침습적 1차 검사)
– CT/MR 혈관조영술: 협착 위치와 범위 확인)
– 캡토프릴 신장스캔(Captopril 99mTc-DTPA scan): ACE 억제제를 투여 후 혈류 저하된 콩팥의 기능 감소 여부를 평가하여 진단에 도움을 줍니다.
캡토프릴 신장스캔(Captopril 99mTc-DTPA scan)
Q . Captopril을 주기 전과 후의 신장 기능 비교
- 신동맥협착(Renal artery stenosis)이 있는 쪽 신장은 혈류 감소로 인해 RAAS 시스템을 활성화시켜 혈압을 억지로 유지합니다.
- 그런데 Captopril은 ACE 억제제로 Angiotensin II 생성을 억제해서, 그동안 혈압을 유지하던 보상기전을 차단합니다.
- 결국 협착된 신장은 혈압 유지 기전이 없어지고, 사구체 여과가 떨어지게 됩니다.


- Renogram (신장 스캔) : 시간에 따른 방사성 동위원소의 신장 내 농도 변화 곡선을
- 정상 신장의 Renogram
- 빠르게 상승했다가 정점에서 하강
→ 방사성 물질이 신장으로 들어왔다가 배출되면서 하강
- 빠르게 상승했다가 정점에서 하강
- 협착된 신장:
- Captopril 전: 비교적 정상이거나 경한 지연
- Captopril 후:
- 방사성 물질이 신장으로 잘 들어가지 못함 -> 정점이 늦게 나타남. 곡선이 천천히 올라감
- 방사성 물질이 신장에서 잘 배출되지 못함 -> 농도값이 올라간 채 유지되며 하강을 천천히 하게됨

Schubert R, Renal artery stenosis. Case study, Radiopaedia.org (Accessed on 23 Jul 2025) https://doi.org/10.53347/rID-14027

[치료]
– 치료의 목표는 혈압 조절과 신기능 보존입니다.
– 생활습관: 금연, 저염식, 체중 조절, 지질 조절
– 약물치료: ACE 억제제/ARB (양측성 협착 시 주의), 이뇨제, CCB 등
– 시술/수술:
• 경피적 신동맥 혈관 성형술(PTA): 주로 섬유근이형성증에 효과적
• 스텐트 삽입: 죽상동맥경화증 환자에서 고려
• 수술적 혈관 재건: 드물게 시행, 다른 방법 실패 시
콩팥정맥혈전증 (Renal Vein Thrombosis, RVT)
– 콩팥정맥 내 혈전 형성으로 신장 혈류 차단
– 신증후군 환자에서 흔히 발생
– 급성은 옆구리 통증·혈뇨, 만성은 무증상
[정의]
– 콩팥정맥혈전증은 신정맥에 혈전이 발생하여 혈류가 차단되는 질환입니다.
– 급성 형태는 급격한 신혈류 차단으로 증상이 뚜렷하고, 만성 형태는 점진적 폐쇄로 무증상일 수 있습니다.
[원인/위험요인]
– 가장 흔한 원인은 신증후군 (특히 막성 사구체신염)
– 그 외 원인: 신장종양, 외상, 탈수(특히 신생아), 혈액 과응고 상태(항인지질 증후군, 단백 C/S 결핍 등)
– 위험요인: 정맥 울혈, 탈수, 감염, 임신·피임약 복용
[임상양상]
– 급성: 옆구리 통증, 혈뇨, 신장 종대, 급성 신부전
– 만성: 무증상인 경우 많으며, 신증후군의 합병증으로 발견
– 양측성일 경우 빠르게 신부전 진행 가능
[진단]
– 기본검사: 소변검사(혈뇨, 단백뇨), 혈액검사(크레아티닌 상승)
– 영상검사: 도플러 초음파 (비침습적 1차 검사)
– CT/MR 혈관조영술: 혈전 위치·범위 확인
– 신정맥조영술: 확진용 gold standard (현재는 잘 사용되지 않음)

Ashraf A, Renal vein thrombosis. Case study, Radiopaedia.org (Accessed on 23 Jul 2025) https://doi.org/10.53347/rID-172664

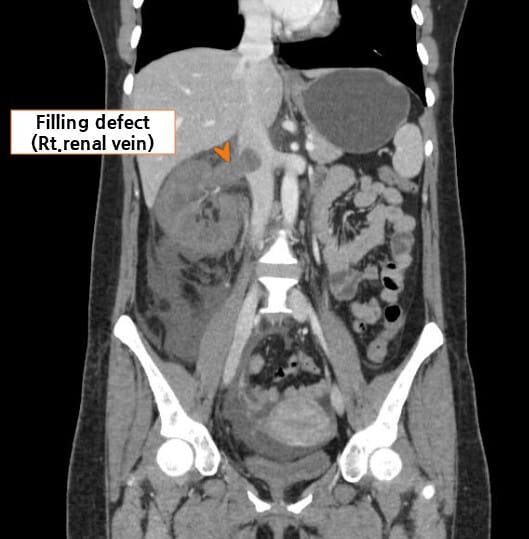
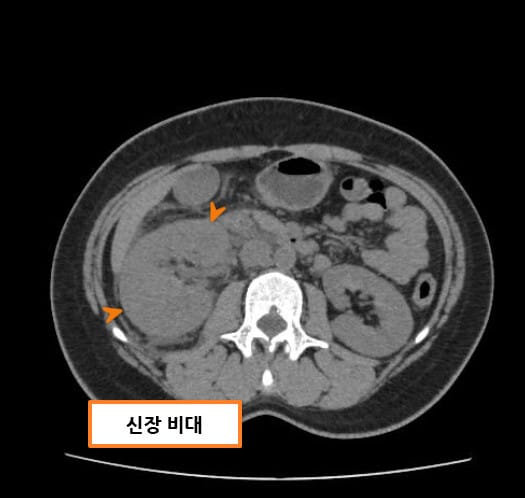
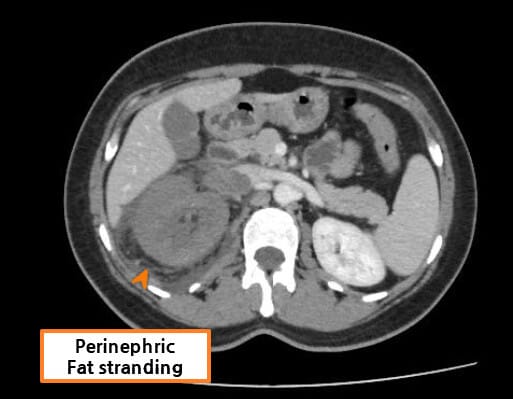
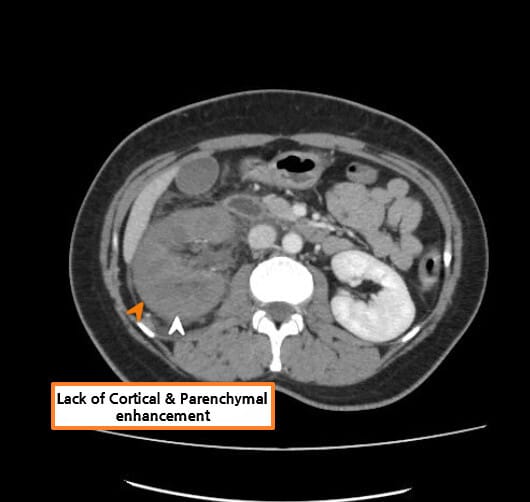

Abdrabou A, Renal vein thrombosis. Case study, Radiopaedia.org (Accessed on 23 Jul 2025) https://doi.org/10.53347/rID-51291
[치료]
– 치료의 목표는 혈전 진행 억제와 신기능 보존입니다.
– 항응고요법: 헤파린 → 와파린 (장기 유지 요법)
– 원인 치료: 신증후군 치료, 종양 제거 등
– 혈전 용해술 또는 수술: 양측성, 급성 진행성, 신부전 동반 시 고려
– 보존적 치료: 혈압 조절, 수분·전해질 균형 유지
혈전 미세혈관병증 (Thrombotic Microangiopathy, TMA)
– 소혈관 내 혈전 형성으로 장기 허혈 유발
– 용혈성 빈혈 + 혈소판 감소 + 장기손상이 3대 특징
– 대표적 질환: TTP, HUS, 약물 유발 TMA
[정의]
– 혈전 미세혈관병증은 소혈관 내 혈전 형성으로 적혈구 파괴와 장기 허혈을 초래하는 임상·병리적 증후군입니다.
– 특징적으로 미세혈관병성 용혈성 빈혈(MAHA), 혈소판 감소증, 장기 기능부전이 동반됩니다.
[원인/위험요인]
– 가장 대표적 원인: 혈전성 혈소판감소성 자반증(TTP), 용혈성 요독 증후군(HUS)
– 약물 유발: Calcineurin 억제제, 항암제, 퀴닌 등
– 이차성 원인: 자가면역질환(SLE, APS), 임신 관련(TTP/HUS), 악성 고혈압, 이식 후 합병증
[임상양상]
– 빈혈 증상: 창백, 피로, 호흡곤란 (적혈구 파괴)
– 출혈 경향: 혈소판 감소로 점상출혈, 멍
– 신장 침범: 혈뇨, 단백뇨, 급성 신손상(HUS에서 뚜렷)
– 신경학적 증상: 혼돈, 경련, 두통 (TTP에서 특징적)
– 발열, 전신 허약감 동반 가능
[진단]
– 혈액검사: 빈혈(Hb↓), 혈소판↓, LDH↑, 빌리루빈↑, Coombs 음성 용혈
– 말초혈액도말: 파편적 적혈구(schistocytes) 확인
– 신기능검사: BUN, 크레아티닌 상승 (HUS)
– 특수검사: ADAMTS13 활성도 감소 (TTP 진단에 중요)
– 영상검사: 비특이적, 장기 허혈 소견
[치료]
a) TTP:
– 지체 없이 혈장교환술을 시작하고 스테로이드를 병합합니다.
– Caplacizumab을 조기에 병합 투여하여 혈소판 회복을 유도할 수 있습니다.
– 재발 위험이 높거나 ADAMTS13 활성이 매우 낮으면 Rituximab을 고려합니다.
b) STEC-HUS:
– 기본적으로 수액·전해질 교정, 투석 등 지지요법을 시행합니다.
– 항생제/항연동제는 일반적으로 피합니다.
c) aHUS
– Eculizumab/Ravulizumab 등 보체 억제제를 표준으로 투여합니다
– 투여 전/중 수막구균 백신 및 예방적 항생제를 고려합니다.
– 약물 유발·임신 관련 TMA는 원인 제거(약물 중단, 분만)와 표준 지지치료를 반드시 시행합니다. 혈소판 수혈은 중증 출혈 시에만 신중히 시행합니다.
– 치료 중에는 용혈 지표, 신기능, 신경증상을 면밀히 모니터링하며, 필요 시 투석을 시행합니다.
요로결석
신장 결석 (Renal Stones, Nephrolithiasis)
극심한 옆구리 산통
혈뇨 동반
[정의]
신장 결석은 소변 내 결석 형성 물질이 응집하여 요로에 돌이 생기는 질환으로, 폐쇄와 통증, 감염을 일으킬 수 있습니다.
[원인/위험요인]
– 가장 흔한 원인은 칼슘 결석(수산칼슘, 인산칼슘)입니다.
– 그 외 요산 결석, 시스틴 결석, 감염(Struvite 결석 – Ureolytic bacteria) 이 있습니다.
– 위험요인: 탈수, 고염분 식이, 고단백 식이, 비만, 통풍, 요로 감염, 가족력
[임상양상]
– 급성 옆구리 산통: 파도치듯 주기적이며 매우 심한 통증 (요관 연동운동 때문)
– 혈뇨: 요로 점막 손상으로 육안적·현미경적 혈뇨 발생
– 배뇨통·빈뇨: 하부 요로 자극 시
– 구역·구토: 교감신경 자극으로 동반 가능
– 요로폐쇄 및 감염 시 발열, 패혈증 위험
[진단]
– 기본검사: 소변검사(혈뇨, 세균), 혈액검사(크레아티닌, 전해질, 요산)
– 영상검사: 비조영 CT (Gold standard)
– KUB X-ray: 방사선 비투과성 결석 확인 가능
– 초음파: 임산부, 소아 등 방사선 노출 제한 환자에서 유용
[치료]
– 치료의 목표는 통증 조절, 결석 배출, 재발 예방입니다.
– 생활습관: 수분 섭취 증가, 저염식, 균형 잡힌 식단
– 약물치료: 진통제(NSAIDs), 알파차단제(Tamsulosin, 요관 이완), 요산 결석 시 Allopurinol
– 시술/수술:
• 체외충격파 쇄석술(ESWL): 작은 결석에 효과적
• 요관내시경적 결석 제거술(URS) • 경피적 신절석술(PCNL): 큰 결석, 복잡한 결석에 사용
• 드물게 개복 수술
요관 결석 (Ureteral Stones)
[임상양상]
– 심한 옆구리 산통(colicky pain)
– 혈뇨, 오심·구토
[치료]
– 소결석: 수분섭취·진통제
– 배출 촉진: 알파차단제
– 난치성: 체외충격파쇄석술(ESWL), 내시경 제거
방광 결석 (Bladder Stones)
하부폐색과 연관
내시경 쇄석·제거가 표준
원인 교정이 재발 예방의 핵심
[정의]
방광 내 결석으로 배뇨말통·요류 중단·혈뇨를 유발합니다.
[원인/위험요인]
– BPH·신경인성 방광·도뇨관 장착이 주요 원인입니다.
[임상양상]
– 간헐적 요류 차단, 회음부 통증, 재발성 UTI가 나타납니다.
[진단]
– 요로 CT/초음파·내시경으로 진단합니다.
[치료]
– 경요도 쇄석/제거(TURL)가 표준
– 감염 동반 시 적절한 항생제를 병행합니다.
– 재발 예방을 위해 BPH 등 기저 원인을 교정합니다.
비뇨기 감염 및 염증
하부요로감염 (Lower UTI: 방광염·요도염)
- 주된 부위: 방광, 요도
- 주요 증상: 배뇨통(dysuria), 빈뇨(frequency), 절박뇨(urgency), 하복부 불편감
- 전신 증상: 거의 없음
- 진단: 소변검사에서 백혈구뇨(pyuria), 세균뇨(bacteriuria), nitrite 양성
- 치료: 경구 항생제 (Nitrofurantoin, TMP-SMX, Fosfomycin 등)
- 예후: 치료 시 합병증 없이 호전됨
상부요로감염 (Upper UTI: 신우신염)
- 주된 부위: 신우, 신실질
- 주요 증상: 발열, 오한, 옆구리 통증(flank pain), 늑골척추각 압통(CVA tenderness), 오심·구토
- 전신 증상: 동반 (패혈증 위험)
- 진단: 소변검사 + 혈액검사(CBC, CRP, ESR), 필요 시 영상검사(초음파, CT)
- 치료: 입원 치료 필요 가능, 정맥 항생제(세팔로스포린, Piperacillin-tazobactam, Carbapenem 등)
- 예후: 지연 시 패혈증, 신부전, 신장 반흔 등 합병증 위험
신우신염 (Pyelonephritis)
상부 요로감염
발열·옆구리 통증·배뇨 증상
[정의]
신우신염은 세균이 방광에서 상행하여 신우와 신실질에 감염을 일으킨 질환입니다.
주로 대장균(E. coli)이 원인균으로, 급성 및 만성 형태로 구분됩니다.
[원인/위험요인]
– m/c : 하부 요로감염에서 상행한 세균 감염
– 요관 결석·구조적 이상·도뇨관 삽입이 위험을 높입니다.
– 여성, 임신, 당뇨병 환자에서 잘 발생합니다.
[임상 양상]
– 발열·오한이 특징적입니다.
– 옆구리 통증과 CVA 압통(늑골척추각 압통)이 나타납니다.
– 배뇨통, 빈뇨, 절박뇨 등 방광염 증상이 동반될 수 있습니다.
– 구역·구토, 전신쇠약이 흔하며, 심한 경우 패혈증으로 진행할 수 있습니다.
[진단]
– 소변 검사: 백혈구뇨, 세균뇨, 아질산염 양성.
– 요 배양: 원인균과 항생제 감수성을 확인합니다.
– 혈액 검사: 백혈구 증가, CRP/ESR 상승.
– 영상: 합병증 의심 시 신장 초음파나 CT에서 수신증·농양 여부를 확인합니다.
[치료]
– 치료의 기본은 적절한 항생제 투여입니다.
– 항생제는 보통 10~14일간 투여하며, 배양 결과에 따라 표적 치료로 전환합니다.
– 충분한 수분 섭취와 해열·진통제를 병행합니다.
a) 외래 치료 가능 환자
– Fluoroquinolone(Ciprofloxacin, Levofloxacin)
– 또는 TMP/SMX를 사용합니다.
b) 입원 치료가 필요한 경우(고열·구토·패혈증 위험)
– 3세대 세팔로스포린(Ceftriaxone),
– Ampicillin+Gentamicin, Piperacillin/Tazobactam 등을 사용합니다.
c) 임산부
– Cephalosporin 계열 항생제를 주로 사용합니다. (FQ 금기)
전립선염 (Prostatitis)
a) 급성: 고열·회음부 통증·배뇨곤란
b) 만성: 반복적 골반통·배뇨증상
급성 세균성 전립선염 (Acute Bacterial Prostatitis)
[정의]
요로 병원체가 전립선에 급성 감염을 일으켜 전신 증상과 하부요로 증상이 동반되는 상태를 말합니다.
[원인/위험요인]
– 주로 E. coli 등 장내세균이 원인이 됩니다.
– 요로기형, 최근 요로 처치, 도뇨관 삽입, 당뇨가 위험을 높입니다.
[임상 양상]
– 발열·오한, 회음부 통증, 배뇨통·빈뇨·급뇨, 때로는 급성 요폐가 동반됩니다.
– 직장수지검사(DRE)에서 전립선 압통·종창이 관찰될 수 있습니다(심한 통증 시 무리한 촉진은 피합니다).
[진단]
– 요검사·요배양으로 원인균과 감수성을 확인합니다.
– 패혈증 의심 시 혈액배양을 시행합니다.
[치료]
– 경험적 정주 항생제 후, 배양 결과에 따라 경구로 전환합니다.
– 권고 항생제: 3세대 세팔로스포린(예: Ceftriaxone), Piperacillin/Tazobactam, 필요 시 Carbapenem을 고려합니다.
– 외래 가능 시 경구 Fluoroquinolone(Ciprofloxacin, Levofloxacin) 또는 TMP/SMX를 사용합니다(감수성 기반).
– 요폐가 있으면 유치도뇨는 감염 악화를 유발할 수 있어 상치골 천자도뇨를 우선 고려합니다.
– 해열·진통, 수분 보충, 배뇨 완화 목적의 알파차단제를 병용할 수 있습니다.
만성 세균성 전립선염 (Chronic Bacterial Prostatitis)
[정의]
3개월 이상 반복되는 골반통·배뇨증상과 간헐적 균뇨가 특징이며, 전립선 분비물/사정 후 소변에서 균이 검출되는 상태입니다.
[임상 양상]
– 배뇨통·회음부 불쾌감·사정통·하복부 통증이 지속·재발합니다.
– 성 기능 저하, 삶의 질 저하가 동반될 수 있습니다.
[진단]
– 요배양, 필요 시 4-컵 또는 2-컵 검사(전립선 마사지 전후 샘플)로 전립선 기원 감염을 확인합니다.
[치료]
– 조직 침투가 좋은 경구 항생제를 충분 기간 사용합니다.
– 권고 항생제: Fluoroquinolone 또는 TMP/SMX(감수성 기반).
– 증상 조절: 알파차단제, 진통제, 온수 좌욕, 골반저 이완 운동 등을 병행합니다.
– 재발이 잦거나 난치성인 경우 비세균성 만성 골반통 증후군 감별과 다학제적 치료를 고려합니다.
방광염 (Cystitis)
급성 세균성 방광염이 가장 흔합니다
재발·임신·남성·도뇨관은 합병성으로 분류합니다
항생제는 지역 내성률·배양 결과에 맞추어 선택합니다
급성 세균성 방광염 (Acute Bacterial Cystitis)
[정의]
방광 점막의 급성 세균감염으로, 건강한 성인 여성에서 가장 흔하게 발생합니다.

여성은 요도가 짧고 항문과의 거리가 가까워 세균(특히 대장균)이 요도를 통해 방광으로 쉽게 침투할 수 있기 때문에 방광염이 더 잘 발생합니다.
[임상 양상]
– 배뇨통·빈뇨·절박뇨·치골상부 불쾌감이 전형적입니다.
– 혈뇨가 동반될 수 있으나 발열·옆구리 통증이 뚜렷하면 상부 감염(신우신염)을 의심합니다.
[진단]
– 요검사에서 백혈구뇨·아질산염 양성이 특징적이며, 재발·임신·비전형 증상에서는 요배양을 권장합니다.
[치료]
Nitrofurantoin과 Fosfomycin은 모두 대장균(Escherichia coli)에 대한 효과가 높고, 장내 정상 세균총 교란이 적어 내성 억제에도 유리합니다.
- Nitrofurantoin은 요로에만 작용하는 국소 항생제로, 전신 흡수는 적고 방광 내에 고농도로 축적되어 단순 방광염에 매우 효과적입니다.
- Fosfomycin 역시 단 1회 복용만으로 방광에 높은 농도로 도달하며, 다제내성균(MDR)에 대해서도 항균력이 뛰어나고 내성률이 낮아 단순 방광염의 1차 치료제로 사용됩니다.
– 단순성(비임신 여성): Nitrofurantoin, Fosfomycin, 또는 TMP/SMX(지역 내 E. coli 내성 낮을 때).
– 합병성(남성, 임신, 당뇨, 구조적 이상, 도뇨관 등): Fluoroquinolone 또는 경구 3세대 세팔로스포린(예: Cefpodoxime) 중심으로 더 긴 기간 치료합니다.
– 임신: Cephalosporin 또는 Amoxicillin/Clavulanate, 상황에 따라 Nitrofurantoin을 고려합니다.
– 도뇨관 관련 감염은 가능하면 카테터 교체·제거를 병행합니다.
– 증상 완화 목적의 진통제와 충분한 수분 섭취를 권장합니다.
간질성 방광염/방광통증증후군 (Interstitial Cystitis/Bladder Pain Syndrome)
[정의]
반복적 배뇨통·빈뇨·야간뇨와 만성 골반통이 지속되지만 세균 배양이 음성인 상태를 말합니다.
[임상 양상]
– 방광 충만 시 통증이 심해지고 배뇨 후 일시적 완화가 나타납니다.
– 방광내시경에서 Hunner 병변이나 점막 출혈이 관찰될 수 있습니다.
[치료]
– 행동치료·방광훈련, 골반저 물리치료, 진통제, 항히스타민제 또는 TCA 계열 약물을 단계적으로 고려합니다.
– 필요 시 방광 내 약물 주입(Heparin, Lidocaine, DMSO)이나 수압확장술을 검토합니다.
– 항생제는 효과적이지 않으므로 사용하지 않으시는 것이 원칙입니다.
요도염 (Urethritis)
배뇨통·요도분비물·자극뇨 증상
임질성(N. gonorrhoeae) vs 비임질성(Chlamydia, M. genitalium 등) 감별
배양/NAAT 결과에 따른 표적 항생제 치료와 파트너 동시 치료
[정의]
요도 점막에 발생한 세균성 또는 비세균성 염증을 말하며, 성매개 병원체가 가장 흔한 원인입니다.
임상적으로 요도분비물, 배뇨통, 빈뇨·절박뇨가 나타나며, 남녀 모두에서 발생하나 남성에서 증상이 더 명확한 경향이 있습니다.
[원인/위험요인]
a) 임질성 요도염: Neisseria gonorrhoeae가 원인입니다.
b) 비임질성 요도염(NGU): Chlamydia trachomatis, Mycoplasma genitalium, Ureaplasma urealyticum, 드물게 HSV 등이 원인입니다.
– 위험요인: 새로운 성파트너 또는 다수 파트너, 콘돔 미사용, 과거 STI 병력, 동반된 요도 카테터·시술 등이 있습니다.
[임상양상]
– 요도분비물: 임질성은 농성·탁한 분비물이 전형적이며, 비임질성은 맑거나 점액성인 경우가 많습니다.
– 배뇨통·자극뇨와 함께 회음부 불쾌감이 동반될 수 있습니다.
– 무증상 감염도 가능하여, 파트너 전파와 상부 요로/생식기 합병증(부고환염, PID) 위험이 존재합니다.
[진단]
– 기본: 요검사에서 백혈구뇨를 확인하고, 요도 면봉 또는 첫 소변으로 NAAT(임질·클라미디아 동시 검사)를 시행합니다.
– 필요 시 분비물 그람염색/배양으로 그람음성 쌍구균(N. gonorrhoeae) 확인을 시도합니다.
– 동반 STI 선별: HIV, 매독, 트리코모나스 등을 상황에 따라 병행합니다.
[치료]
치료의 목표는 증상 해소·전파 차단·합병증 예방입니다.
(A) 임질성 요도염 -> 확진했거나 강력하게 의심될 때
– Ceftriaxone으로 시작하고,
– Chlamydia 병합 가능성을 고려하여 Azithromycin 또는 Doxycycline을 병용합니다.
(B) 비임질성 요도염(NGU):
– 1차로 Doxycycline을 사용하며
–M. genitalium이 의심되거나 재발 시 Azithromycin 또는 Moxifloxacin을 고려합니다.
– 파트너 동시 치료·성관계 회피(치료 완료·증상 소실까지)·치료 후 재검사/재평가를 권장드립니다.
– if) 임신 중이라면
Azithromycin 또는 Amoxicillin을 상황에 맞게 선택하며 테트라사이클린계는 피하시는 것이 원칙입니다.
비뇨 생식기 종양
신장 종양 (Renal Tumors)
대표: 신세포암, 윌름스 종양, 상부요로 이행상피암
공통 3대 증상: 혈뇨·옆구리 통증·복부 종괴
치료는 병기·위험도·신기능을 종합해 수술·전신치료·국소치료를 선택
신장 낭종의 악성 위험도 (Bosniak Classification)
신장 낭종의 악성 위험도 (Bonsiak Classification)
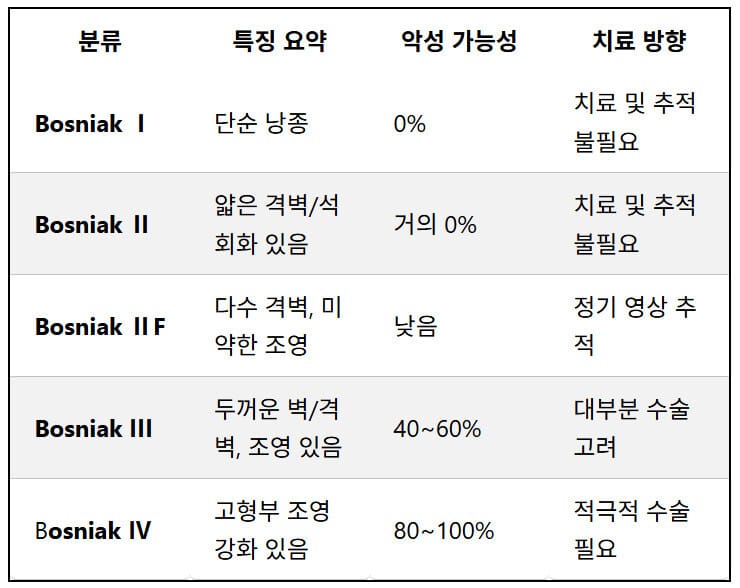

위 분류체계를 통해 신장 낭종의 영상학적 소견을 기준으로 악성 위험도를 평가하고, 치료 방향을 결정할 수 있습니다. 총 5단계(Ⅰ, Ⅱ, ⅡF, Ⅲ, Ⅳ)로 구분하며, 단계가 높을수록 악성 가능성이 증가합니다
[ Bosniak I ]
: 벽이 얇고 격벽, 석회화, 조영증강이 전혀 없는 단순 낭종. 100% 양성



Cuete D, Renal cyst – Bosniak I. Case study, Radiopaedia.org (Accessed on 28 Apr 2025) https://doi.org/10.53347/rID-27479
[ Bosniak II ]
: 얇은 격벽이 있거나, 벽 또는 격벽에 미세 석회화가 있음. 조영증강은 없음.



Haouimi A, Renal cyst – Bosniak class II. Case study, Radiopaedia.org (Accessed on 28 Apr 2025) https://doi.org/10.53347/rID-180354
[ Bosniak IIF (follow-up) ]
: 격벽이 다소 많거나, 벽/격벽에 경미한 조영증강이 있으나 고형 부위 없음. (악성 위험도는 낮지만, 완전히 배제되진 않아 정기적 f/u 필요)


Botz B, Renal cyst – Bosniak type IIF (CEUS). Case study, Radiopaedia.org (Accessed on 28 Apr 2025) https://doi.org/10.53347/rID-72117
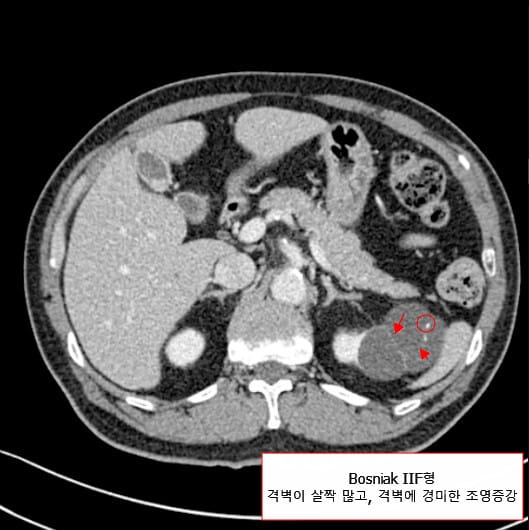
Bickle I, Renal cyst – Bosniak IIF. Case study, Radiopaedia.org (Accessed on 28 Apr 2025) https://doi.org/10.53347/rID-24068
[ Bosniak III ]
: 두꺼운 벽 또는 격벽이 있으며 조영증강이 확인됨. 고형 부위는 없음.
(악성 가능성 40~60%. 대부분 수술적 절제 고려.)



[ Bosniak IV ]
: 낭종 내에 조영증강되는 고형 부위가 존재함. 대부분 신세포암으로 간주.


Bickle I, Renal cyst – Bosniak IV. Case study, Radiopaedia.org (Accessed on 28 Apr 2025) https://doi.org/10.53347/rID-24244

Niknejad M, Renal cyst – Bosniak IV. Case study, Radiopaedia.org (Accessed on 28 Apr 2025) https://doi.org/10.53347/rID-82556
- Bosniak 분류 1, 2형은 추적 관찰하며,
- 3형 이상은 악성 가능성 있어 수술을 고려합니다.
신세포암 (Renal Cell Carcinoma, RCC)
[정의]
-성인에서 가장 흔한 신장 악성종양
–근위세뇨관 상피 기원입니다.
[원인/위험요인]
– 흡연과 비만·고혈압이 대표 위험요인입니다.
– Von Hippel-Lindau 질환 : 유전적 돌연변이에 의해 다발성 신장 종양
– 장기 이식 후 면역억제로 위험이 증가
– 직업성 노출(석유·중금속)과 만성 신질환/장기간 투석 환자에서도 위험이 상승합니다.
[임상양상]
– TrIad : 1) 혈뇨·2) 옆구리 통증·3) 복부 종괴
– EPO 분비로 인한 적혈구증가증·발열·체중감소 같은 Paraneoplastic 소견이 동반될 수 있습니다.
– 신정맥/하대정맥 침범 시 좌측 정계정맥류 악화가 나타날 수 있습니다.
[진단]
– 조영증강 CT 또는 MRI로 고형 종괴의 조영증강 패턴을 평가합니다.
조영증강 영상에서 고형성 종괴 + 중심 괴사, 혈관 침범
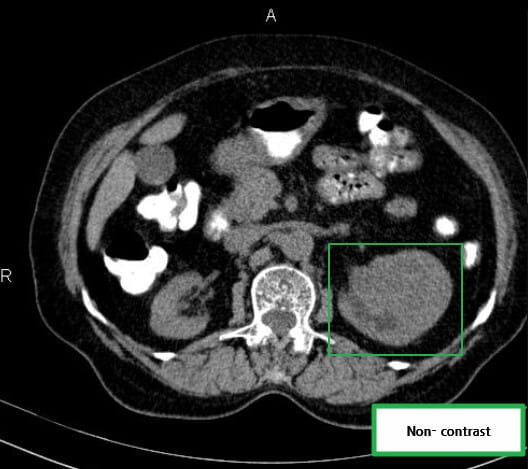
Niknejad M, Renal cell carcinoma. Case study, Radiopaedia.org (Accessed on 07 May 2025) https://doi.org/10.53347/rID-84360
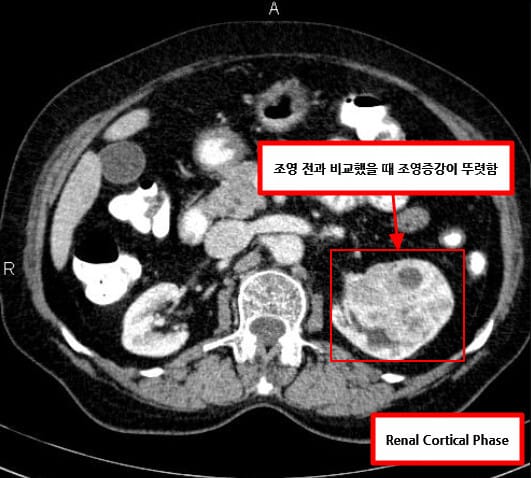
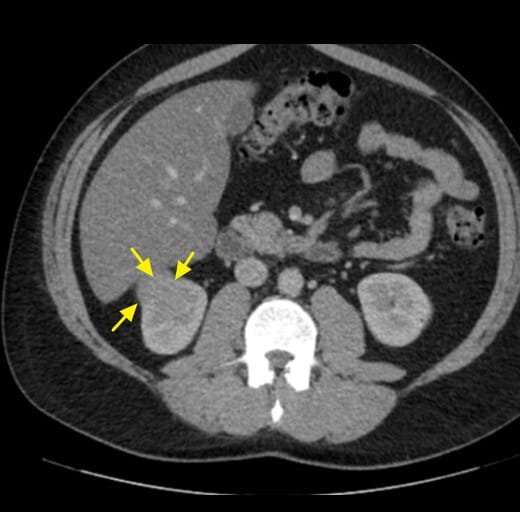
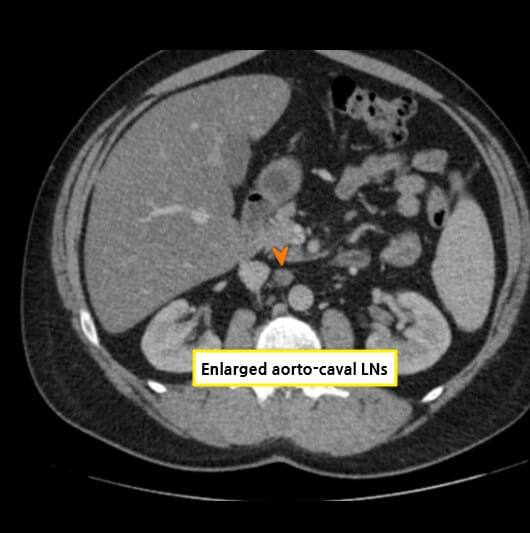
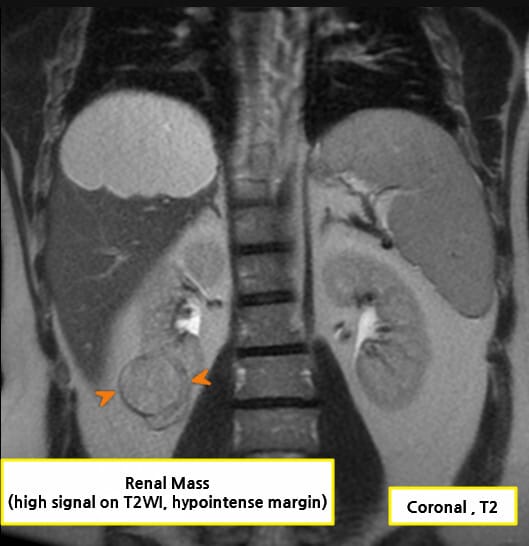

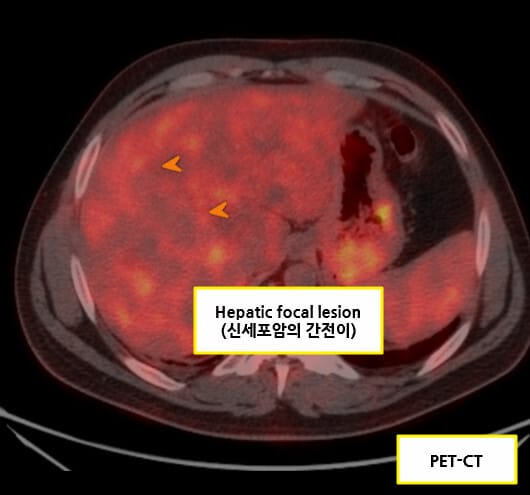
– 복부 초음파 상 고형종괴, 낭성 병변 내 solid component , +(도플러 혈류 증가 가능, 필수는 아님, 신장 외부로의 돌출 및 변형)
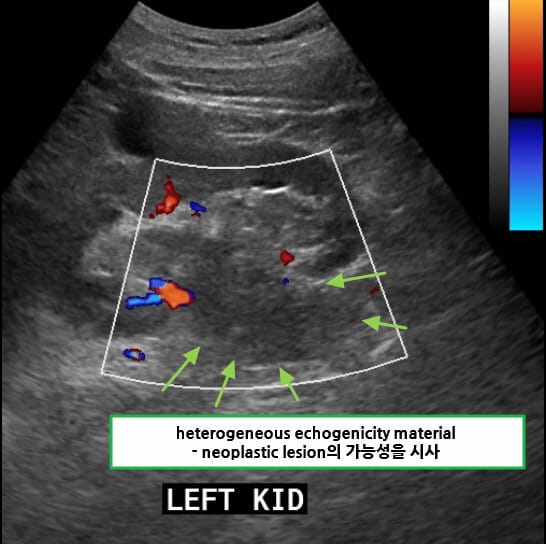


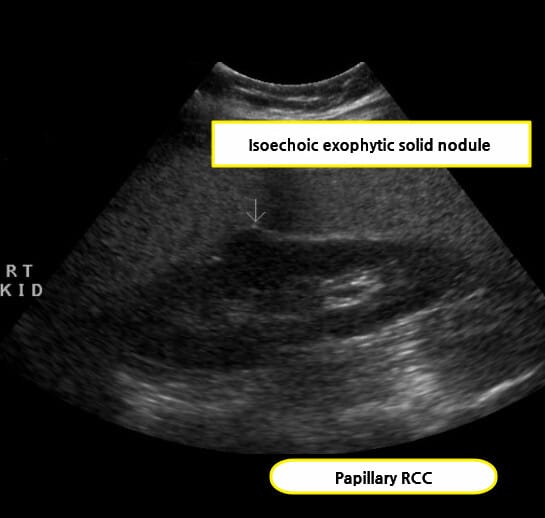
– 신장생검은 작은 종양에서 적극적 감시나 비수술 치료를 고려할 때 진단적 가치가 큽니다.
– 전이 평가를 위해 흉부 CT, 필요 시 뼈/뇌 영상까지 단계적으로 시행합니다.
[Renal cell carcinoma 병기]
신세포암(Renal cell carcinoma, RCC)의 병기는 종양의 크기와 신장을 넘는 침범 정도, 림프절 전이 여부, 원격 전이 여부에 따라 TNM Staging 체계로 분류합니다. 병기는 예후 예측과 치료 결정에 매우 중요합니다.
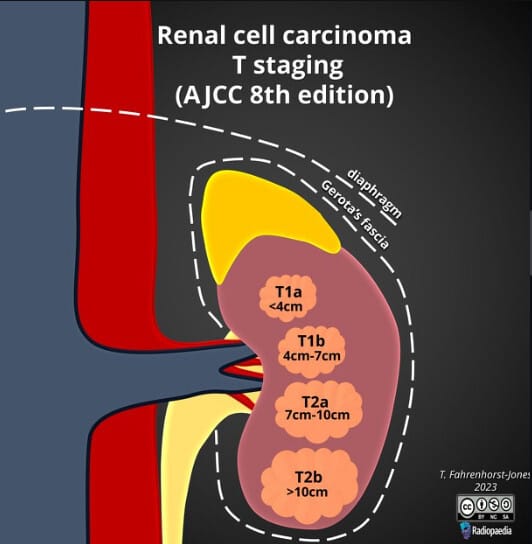
Fahrenhorst-Jones T, Renal cell carcinoma T staging (AJCC 8th edition). Case study, Radiopaedia.org (Accessed on 07 May 2025) https://doi.org/10.53347/rID-177572
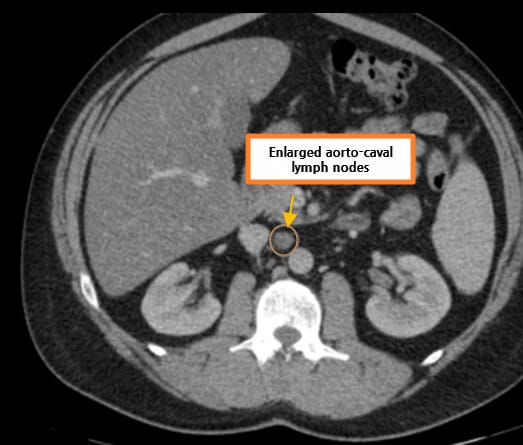
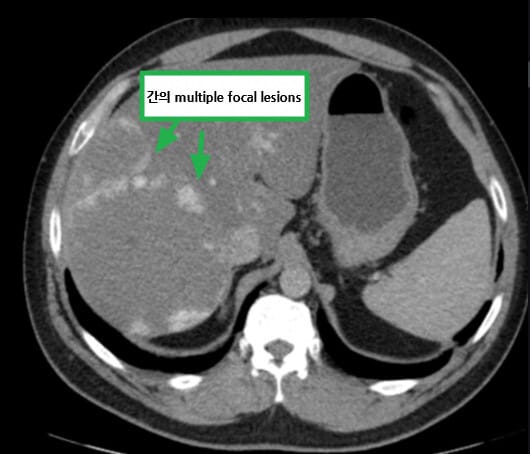

[치료]
- Stage I~II는 국소 질환으로 간주되어 수술적 절제를 우선 시행함
- Stage III는 국소 진행
- Stage IV는 전이성 질환으로 면역치료와 표적치료가 중요합니다.
1) 국소병기(T1~T2): 부분 신절제술(Nephron-sparing)이 원칙이며, 위치·기술적으로 불가하면 근치적 신절제를 시행합니다.
– 고령·동반질환·작은 저위험 종양(T1a)에서는 능동 감시 또는 냉동/고주파 소작 같은 국소치료를 고려합니다.
– 정맥 혈전 동반 시 혈전제거를 동반한 신절제가 필요합니다.
2) 수술 후 병리 고위험(pT2 이상, 양성 절제연 불가, 림프절 전이 등)에서는 선택적으로 보조적 면역치료를 고려합니다.
3) 전이성(mRCC): 위험도(IMDC) 기반으로 면역관문억제제 병용(예: PD-1 + CTLA-4) 또는 TKI(+/− 면역)(axitinib, cabozantinib, lenvatinib 등) 요법을 1차로 사용합니다.
4) 증상 완화·면역치료 반응 최적화를 위해 선택적 감축 신절제술이나 전이 절제를 개별화하여 시행합니다.
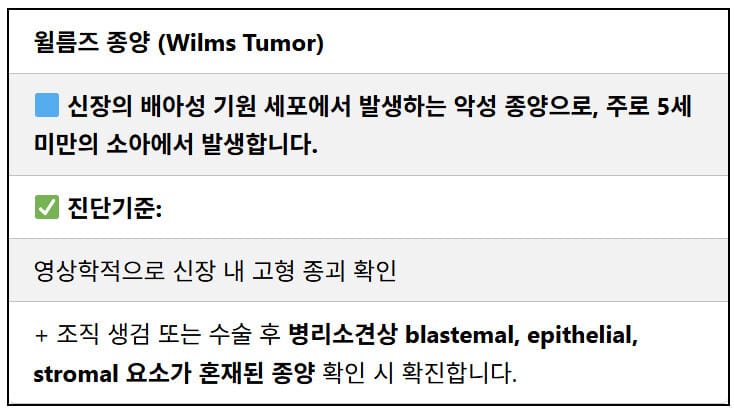
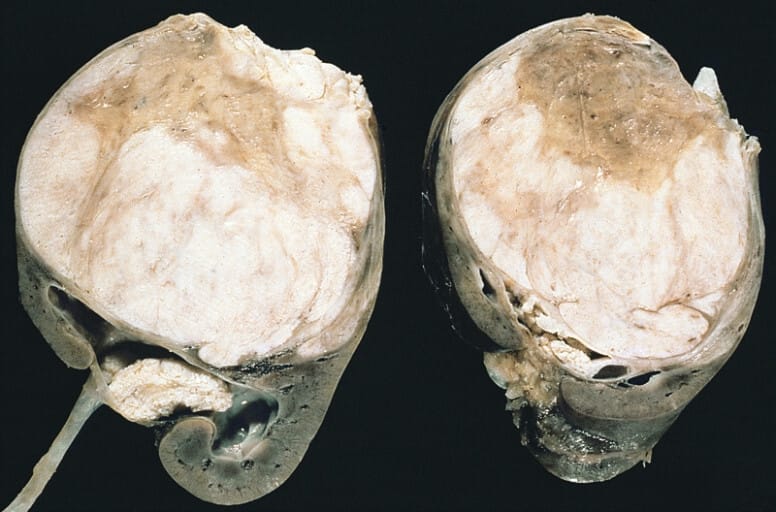
윌름스 종양 (Wilms Tumor, 신아세포종)
[정의]
소아에서 가장 흔한 신장 원발 악성종양으로 배아성 간엽 기원입니다.
통상 3~4세에 진단되며, WT1 변이·WAGR/Denys–Drash 등 유전 증후군과 연관될 수 있습니다.
[원인/위험요인]
– 선천성 기형(무홍채증, 반신비대 등)과 특정 유전자 이상이 위험을 높입니다.
– 가족력은 드물지만 존재 시 조기 선별이 권장됩니다.
[임상양상]
– 보호자가 만지는 무통성 복부 종괴가 가장 흔합니다.
– 혈뇨·복통·고혈압·빈혈·발열이 동반될 수 있습니다.
– 폐 전이가 흔해 기침·호흡곤란으로 발견되기도 합니다.
[진단]
– 복부 초음파로 시작하여 조영증강 CT/MRI로 병기·양측성 여부를 평가합니다.
-CT : 불균일한 고형종괴, Claw sign (정상 신장 실질이 종양을 감싸는 모습) , 폐전이 소견 가능
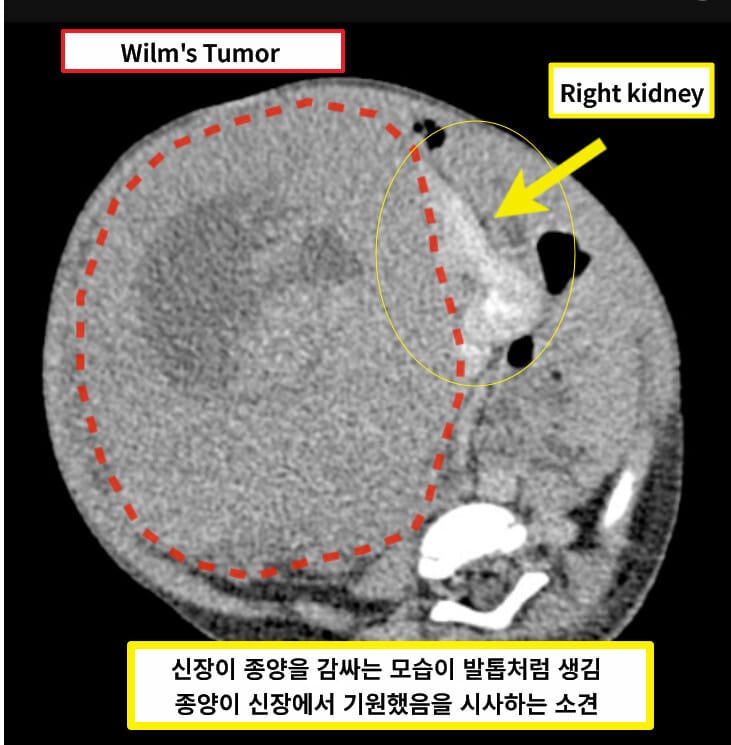
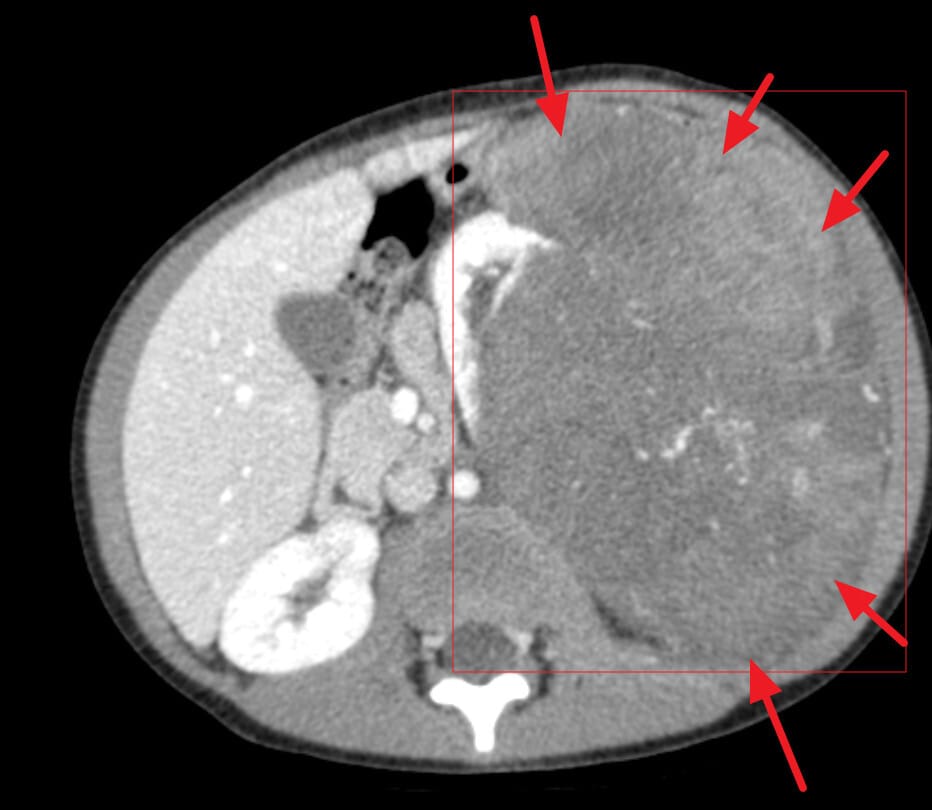
Gaillard F, Wilms tumor. Case study, Radiopaedia.org (Accessed on 24 May 2025) https://doi.org/10.53347/rID-5957
– 흉부 CT로 폐 전이를 확인하며, 조직학적 위험도(유리질변성 유무 등)를 병리로 확정합니다.
– 복부 X -ray : 복강 내 장기 밀림
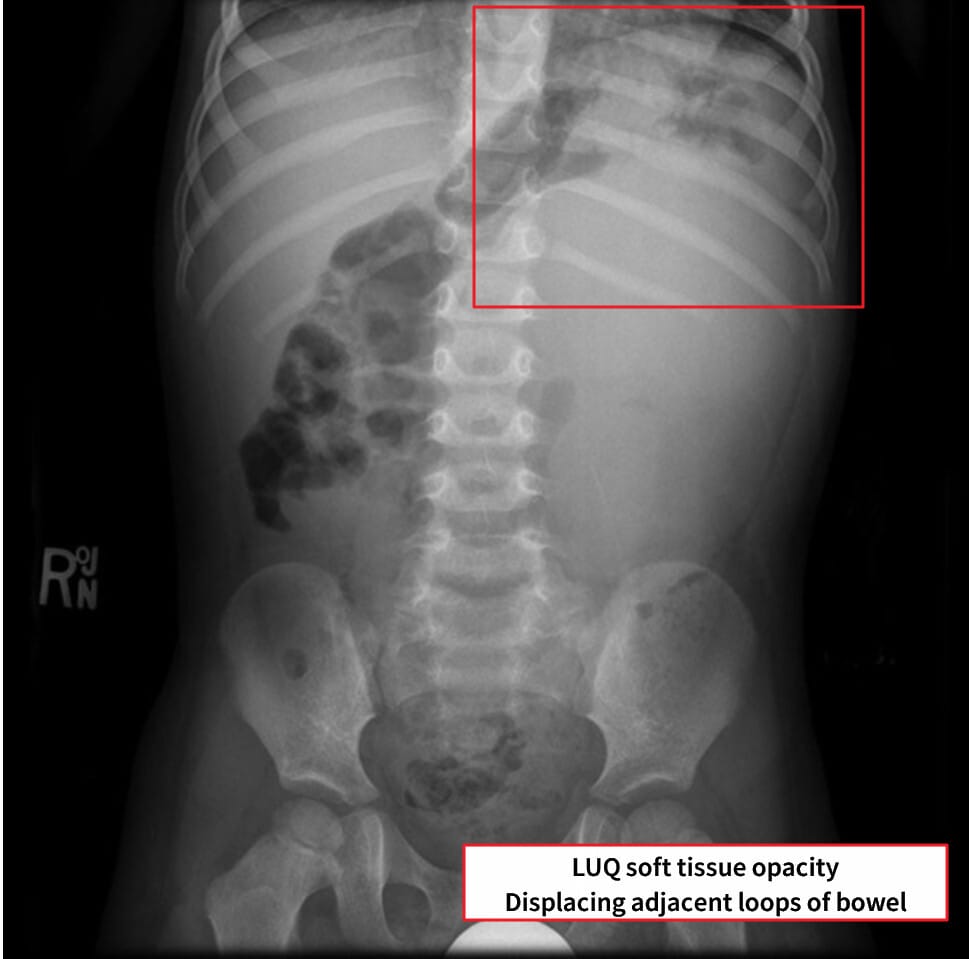
-병리학적 소견
: 신장에서 미분화된 배아세포(blastemal), 상피(epithelial), 간질(stromal) 요소가 함께 관찰됨.
[치료]
– 단측성 국소병기: 근치적 신절제 + 림프절 표본 채취가 표준
– SIOP(유럽) 프로토콜에서는 선행 화학요법(vincristine+dactinomycin±doxorubicin) 후 수술을, COG(북미)에서는 수술 후 보조 화학요법을 기본으로 합니다.
– 고위험 병리 또는 잔존·파열·정맥 침범·폐 전이 시 방사선치료를 병합합니다.
– 양측성·신기능 보존 필요 시 선행 화학요법 후 부분 신절제로 신실질을 최대한 보존합니다.
– 재발 시 구제요법(변경 화학요법, 수술/방사선 재시행)을 개별화합니다.
신우·요관 이행상피암 (Upper Tract Urothelial Carcinoma, Renal Pelvis/Ureter)
[정의]
신우와 요관의 이행상피세포에서 발생하는 요로상피암으로, 방광암과 동일한 기원을 가지며 병태생리가 유사하지만 발생 위치가 다릅니다.

- 신우(renal pelvis) 또는 요관(ureter)의 이행상피(transitional epithelium)에서 발생하는 악성 종양.
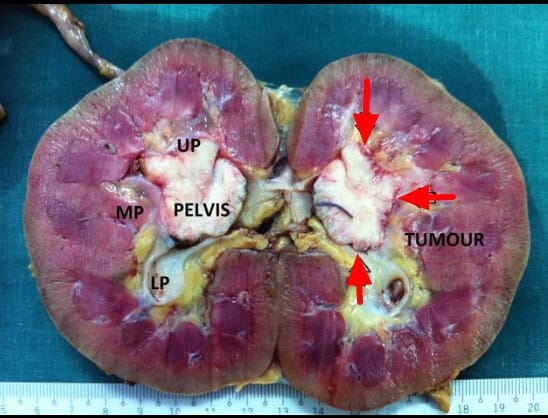
- Renal Pelvis의 Tumor
[원인/위험요인]
– 흡연, 방향족 아민 등 직업성 발암물질 노출이 대표적입니다.
– 진통제 남용, 요로감염·요석, 요로상피암의 과거력, 중국약재 aristolochic acid 노출이 위험을 높입니다.
[임상양상]
– 무통성 간헐적 혈뇨와 요관 침범 시 산통성 옆구리 통증이 흔합니다.
– 상부요로 폐쇄로 수신증이 동반될 수 있습니다.
[진단]
– CT 요로조영술(CT urography)이 1차 영상입니다.
– 요세포검사 및 요관경을 통한 생검으로 확진하고, 위험도(저·고위험)를 분류합니다.
[치료]
(1) 고위험
(고등급, 침윤 의심, 다발/재발, 수신증 동반)
: 신요관절제술 + 방광 cuff 절제가 표준, 항암치료 병합
(2) 저위험
(저등급, 단일, 작고 유두형)
: 신보존 내시경 절제(레이저 절제/생검) 후 국소 화학요법을 선택적으로 시행합니다.
–Neoadjuvant 백금기반 화학요법(Cisplatin+Gemcitabine)을 주로 사용하며 신기능 저하시 Carboplatin으로 대체할 수 있습니다.
-수술 후 병리 고위험 pT2+에서는 신기능이 허용되면 보조 화학요법을 시행합니다.
– 진행/전이성
: cisplatin 기반 1차 후 유지 면역요법 또는 면역관문억제제(PD-1/PD-L1)
항체약물접합체, FGFR 변이 시 표적치료 등을 단계적으로 적용합니다.
– 방광내 재발 예방을 위해 수술 직후 단회 방광내 항암 주입(예: mitomycin)을 고려합니다.
신혈관근지방종 (Angiomyolipoma, AML)
[정의]
혈관·평활근·지방으로 구성된 양성 간엽성 종양입니다.
결절성 경화증(TSC)과 연관된 다발성 형태가 존재합니다.
[원인/위험요인]
– TSC의 TSC1/2 변이와 연관됩니다.
– 임신·에스트로겐 노출 시 성장·출혈 위험이 증가합니다.
[임상양상]
– 대부분 무증상이지만, 출혈 시 급성 옆구리 통증·혈뇨·쇼크가 발생할 수 있습니다.
– 대형 병변은 촉지 종괴·압박 증상을 유발합니다.
[진단]
– CT/MRI에서 지방 성분(−HU) 확인
– 지방이 적은 변이형(“fat-poor”)은 RCC와 감별 위해 생검이 필요할 수 있습니다.
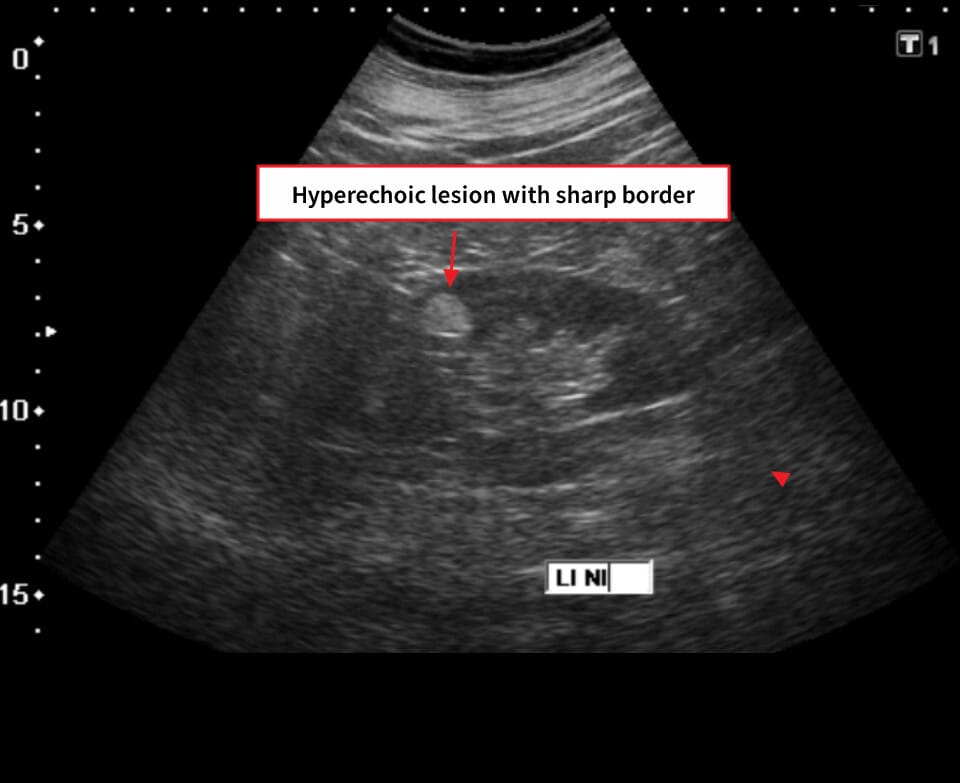
Schubert R, Renal angiomyolipoma. Case study, Radiopaedia.org (Accessed on 19 May 2025) https://doi.org/10.53347/rID-16842
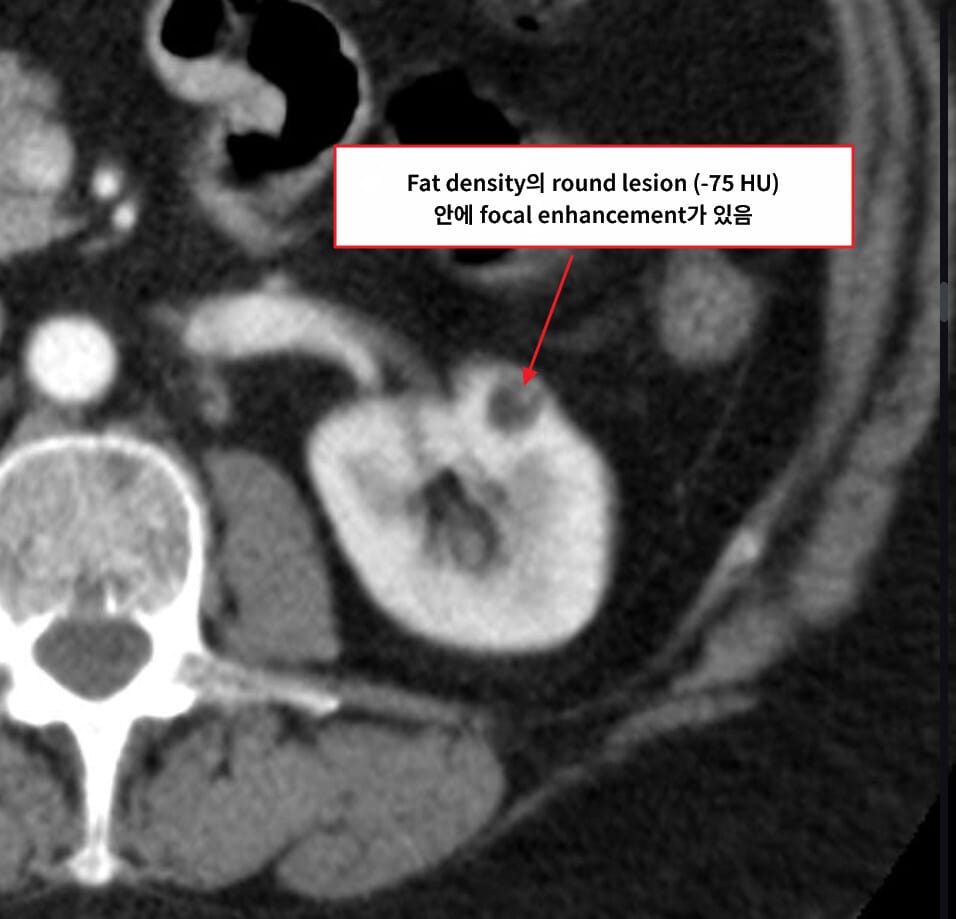
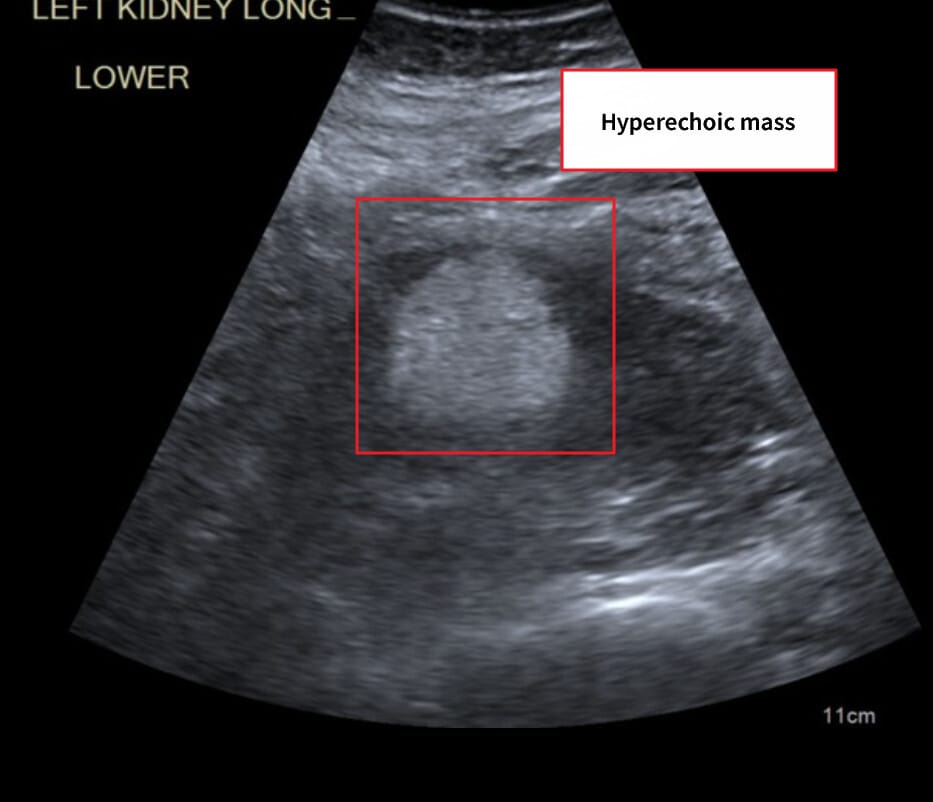
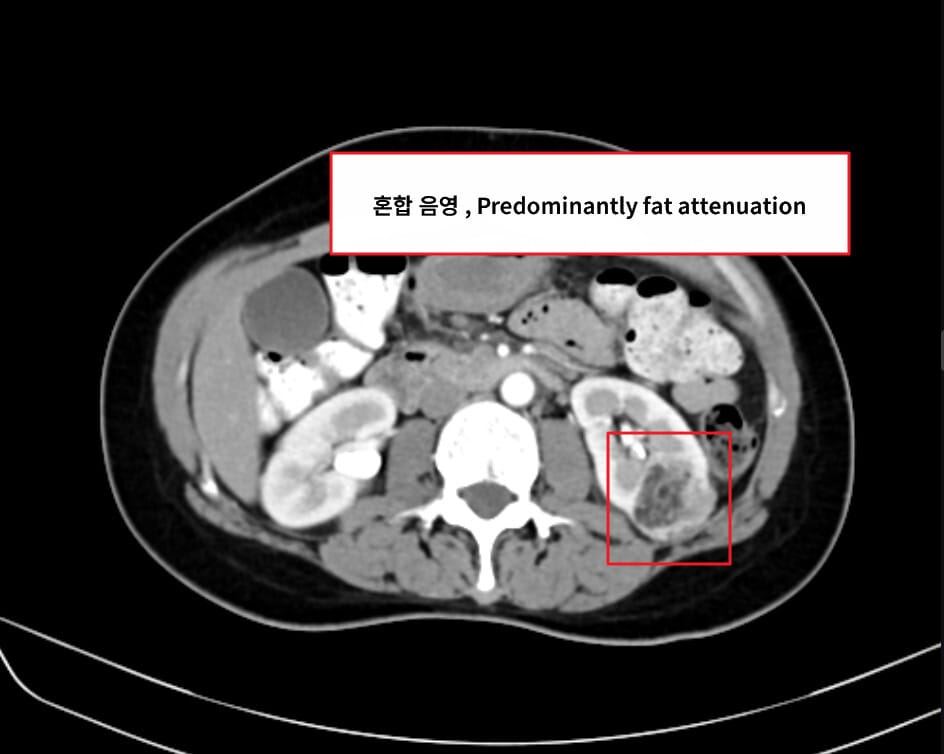
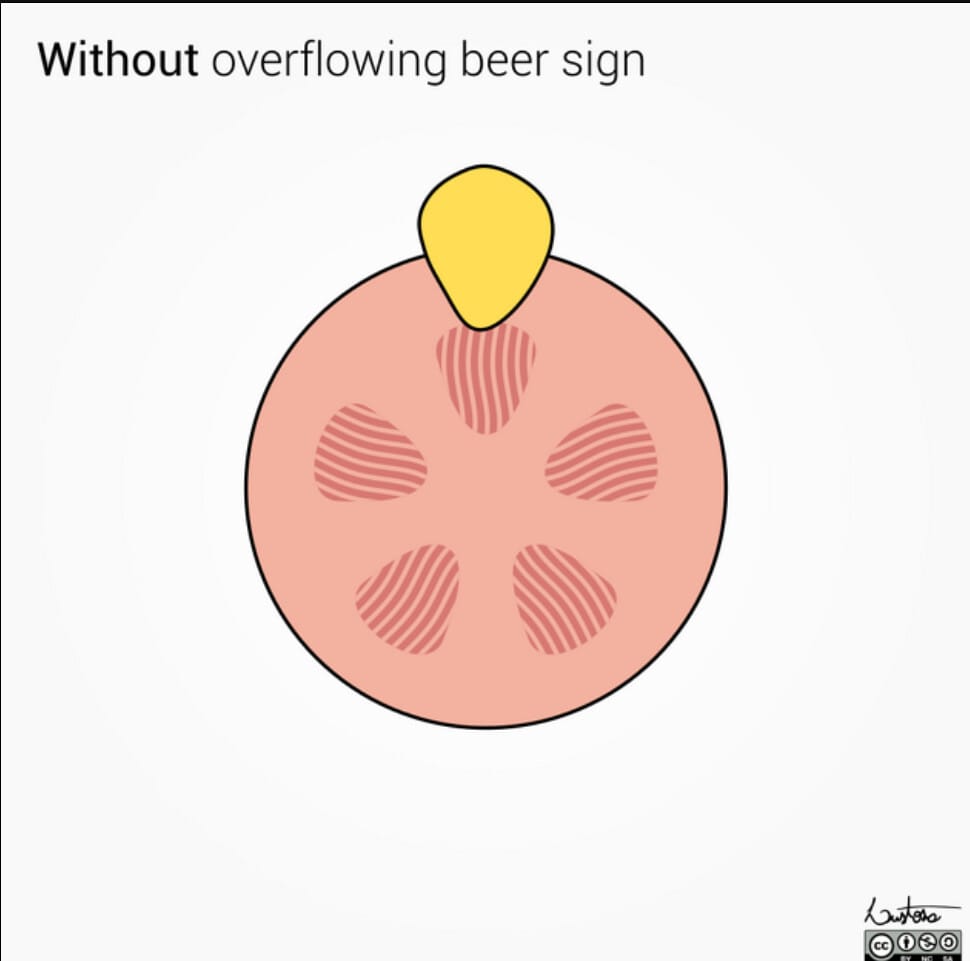
Renal Cell Carcinoma와 감별
–Overflowing beer sign
신장 변연부에 돌출된 병변이 맞닿는 면적이 3mm 이상이면 Renal cell carcinoma 보다 Fat poor angiomyolipoma를 시사합니다.
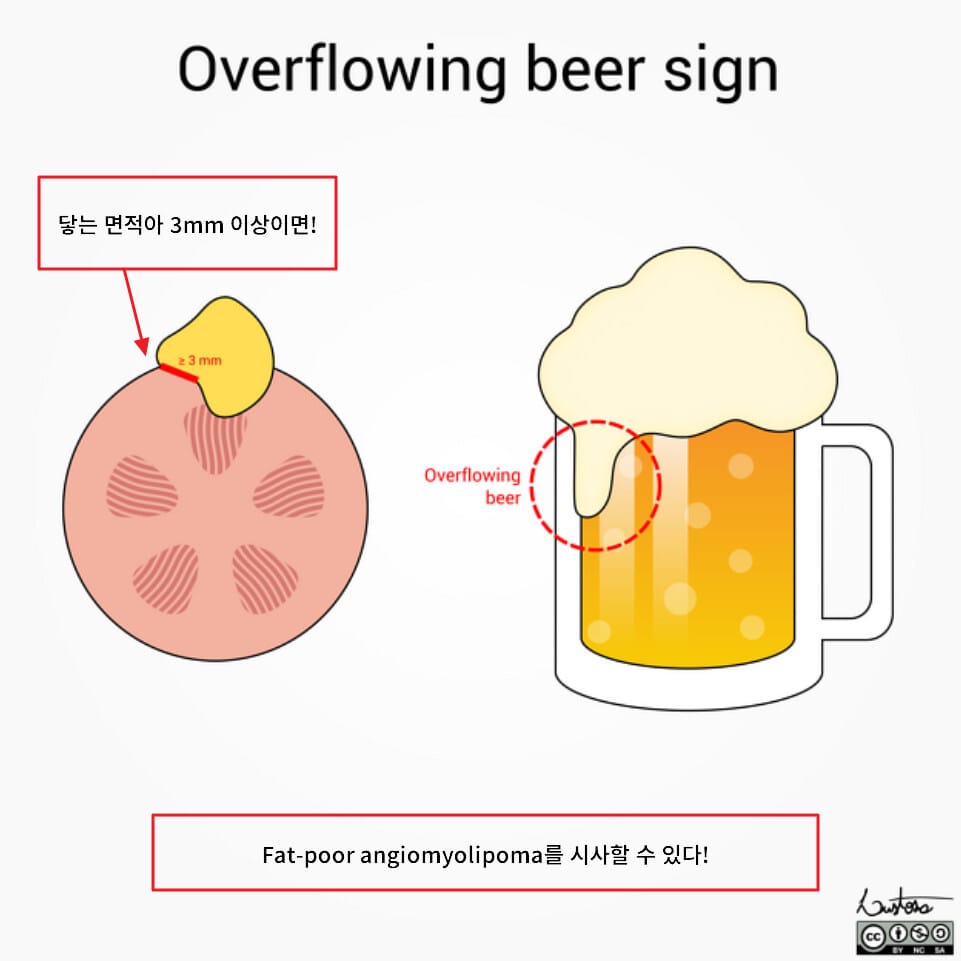
Lustosa L, Overflowing beer sign (illustration). Case study, Radiopaedia.org (Accessed on 19 May 2025) https://doi.org/10.53347/rID-171972
[치료]
– 무증상·저위험: 정기 영상 관찰합니다.
– 유증상·고위험(큰 크기, 동맥류 동반, 임신 계획)
: 선택적 동맥 색전술로 출혈을 예방합니다.
– 국소 절제가 필요하면 부분 신절제를 시행합니다.
– TSC 연관·다발성에서는 mTOR 억제제(everolimus 등)로 크기 감소와 출혈 위험을 줄입니다.
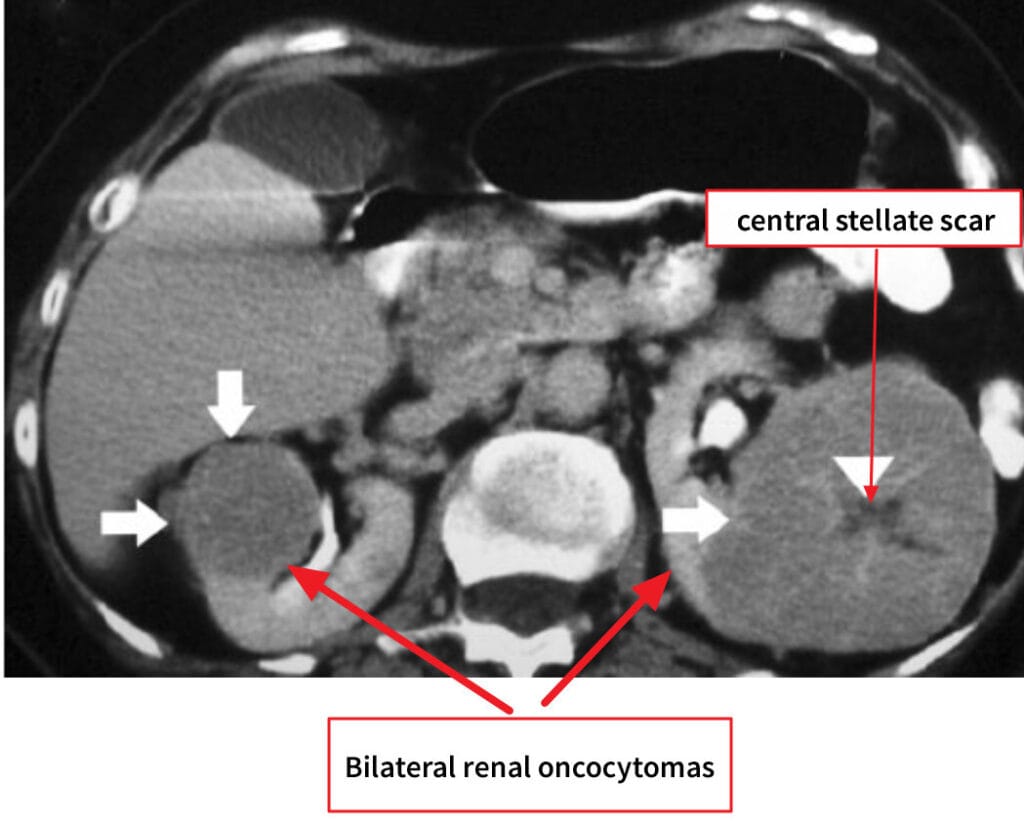
Renal Oncocytoma
[정의]
미토콘드리아가 풍부한 집합관 유래의 양성 상피성 종양입니다.
영상학적으로 RCC(특히 chromophobe)와 감별이 어려울 수 있습니다.
[원인/위험요인]
– 명확한 환경 위험요인은 제한적이며, 드물게 Birt–Hogg–Dubé 증후군과 연관됩니다.
[임상양상]
– 대부분 무증상 우연 발견
– 드물게 혈뇨·옆구리 불편감을 유발합니다.
[진단]
– CT/MRI에서 중심성 반흔이 보일 수 있으나 특이적이지 않습니다.
– 생검으로 진단을 시도하되, 불확실 시 신보존 수술을 고려합니다.
[치료]
– 작은, 확실한 양성 의심 병변은 능동 감시가 가능합니다.
– 감별 불가·성장·증상 시 부분 신절제를 우선합니다.
– 다발성 또는 기능 보존 필요 시 국소 열치료(냉동/고주파)를 선택적으로 고려합니다.
Metanephric Adenoma
[정의]
소형의 양성 신장 상피성 종양으로, 종종 우연히 발견됩니다.
[원인/위험요인]
– 드문 종양으로 뚜렷한 위험요인이 규명되어 있지 않습니다.
[임상양상]
– 대부분 무증상입니다.
– 드물게 혈뇨·통증을 유발할 수 있습니다.
[진단]
– 영상 소견이 비특이적이라 생검/절제 후 병리로 확정하는 경우가 많습니다.
[치료]
– 크기가 작고 확실히 양성으로 판단되면 관찰이 가능합니다.
– 확진·감별 또는 성장 시 부분 신절제로 치료하며 예후는 매우 양호합니다.
Renal Papillary Adenoma
[정의]
직경이 작은 저등급 양성 병변으로, 주로 고령 또는 만성 신질환 환자에서 우연히 발견됩니다.
[원인/위험요인]
– 만성 신손상·장기 투석과의 연관이 보고되어 있습니다.
[임상양상]
– 증상을 일으키지 않는 경우가 대부분입니다.
[진단]
– 영상으로 구분이 어려워 병리에서 작은 크기·저등급 기준으로 판정됩니다.
[치료]
– 우연히 동반 발견되는 경우가 많아 관찰이 원칙입니다.
– 동반 악성종양 감별이 필요하면 해당 병변에 준해 수술적 처치를 합니다.
방광암 (Bladder Cancer)
– 무통성 육안적 혈뇨가 가장 흔한 초기 증상
– 대부분 요로상피암(Transitional Cell Carcinoma, Urothelial carcinoma)
– 흡연이 가장 중요한 위험 인자
[정의]
– 방광의 요로상피에서 발생하는 악성 종양으로, 전체 방광암의 90% 이상을 차지하는 형태는 요로상피암(urothelial carcinoma)입니다.
– 종양은 점막에서 시작하여 점차 방광 근육층 및 주변 장기로 침윤할 수 있습니다.
[원인/위험요인]
– 가장 흔한 원인은 흡연입니다 (담배 속 발암물질이 소변으로 배설되면서 방광 점막에 지속적 노출).
– 직업적 발암물질(아릴아민, 고무·염료·석유화학 산업 노출).
– 만성 방광염, 방광 결석, Schistosoma(주혈흡충) 감염(특히 편평상피암 유발).
– 방사선치료나 항암제(Cyclophosphamide) 과거력
[임상양상]
– 가장 특징적인 증상은 무통성 육안적 혈뇨입니다.
– 빈뇨, 배뇨통, 잔뇨감 같은 자극 증상이 동반될 수 있습니다.
– 진행 시 골반통, 수신증(요관 폐쇄), 체중 감소 등 전신 증상이 나타날 수 있습니다.
[진단]
– 소변검사: 혈뇨 확인.
– 소변세포검사: 암세포 확인 가능.
– 방광경검사(Cystoscopy): 진단의 gold standard, 직접 종양 확인 및 조직생검 가능.
– 영상검사(CT urography, MRI): 종양의 범위 및 전이 평가.
– 병리검사: 요로상피암(urothelial carcinoma), 편평상피암, 선암 등 조직학적 아형 구분.
방광암을 초기에 평가할 때 가장 흔히 시행
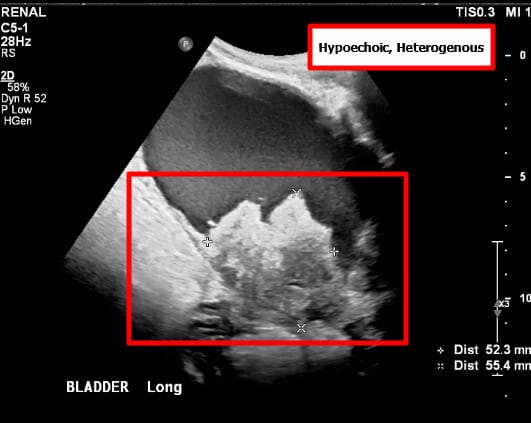
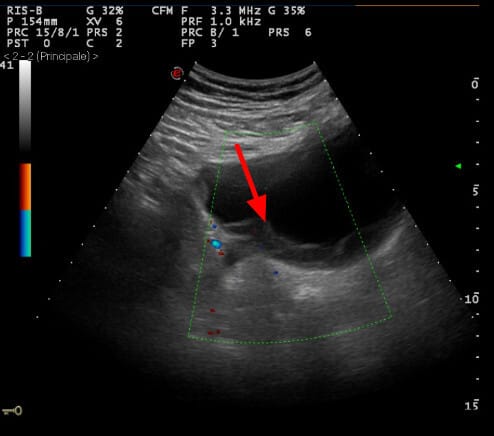
요로조영술 (Intravenous Urography, IVU)
조영제를 통해 요로계 구조를 간접적으로 시각화
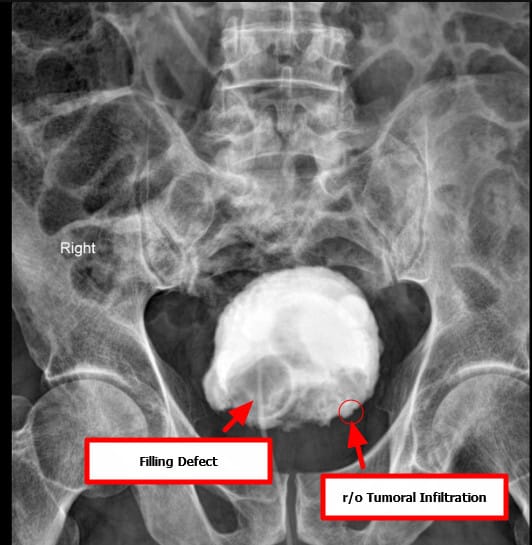
CT
방광암의 병기 결정과 전이 평가에 가장 유용
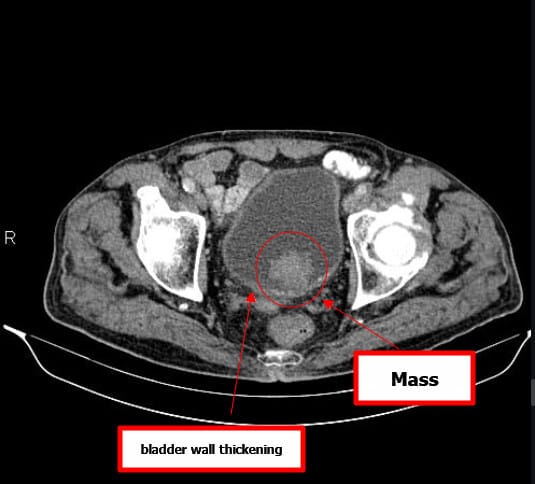
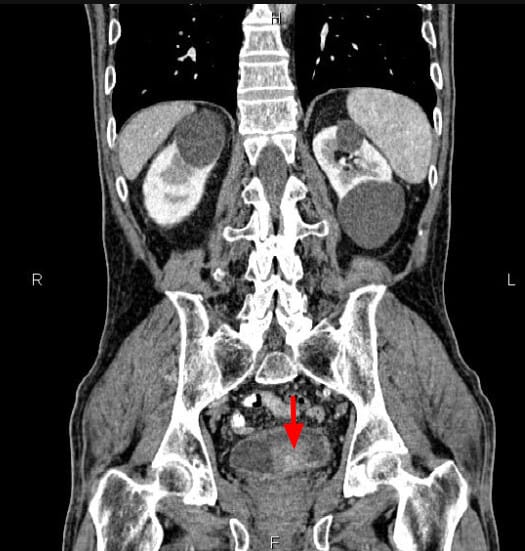
MRI (Magnetic Resonance Imaging)
연부조직 대비가 뛰어나 방광 침윤 깊이를 정밀하게 파악
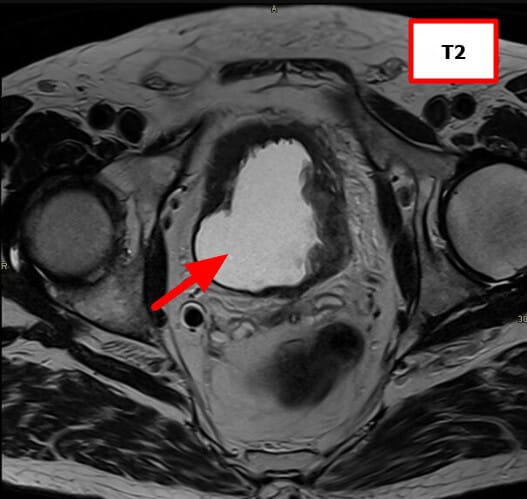
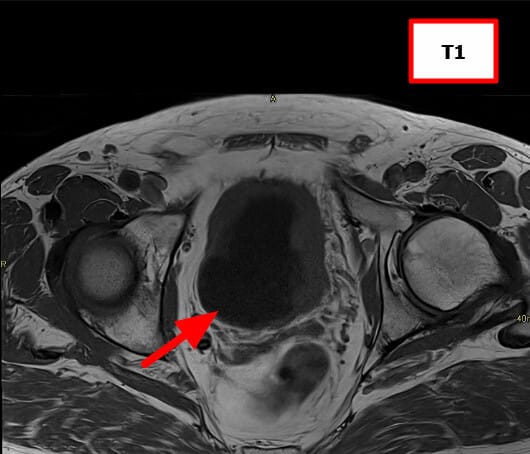
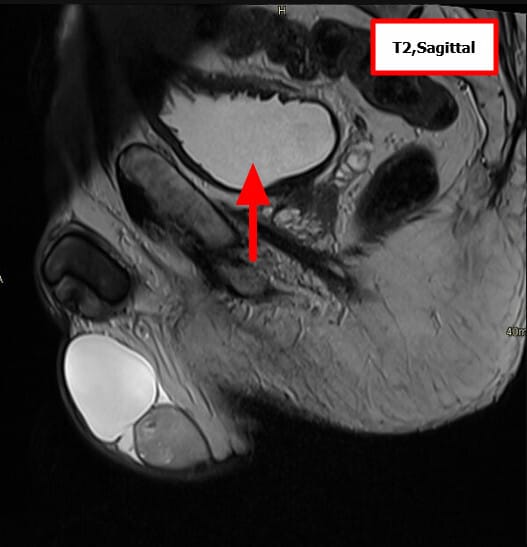
[치료]
– 치료의 목표는 종양 제거와 재발·진행 억제입니다.
- 근육층을 침범하지 않은 비근침윤성암(NMIBC)은 TUR-BT 후 방광 내 BCG 주입이 권장됩니다. 반면, 침윤성 암(MIBC)은 방광 전절제술을 시행합니다.
(A) 비근침윤성 방광암(NMIBC)
: 경요도 방광종양 절제술(TURBT) + 방광내 항암제/BCG 주입.
(B) 근침윤성 방광암(MIBC)
: 근치적 방광절제술(Radical cystectomy) + 골반 림프절 곽청술.
– 국소 진행/전이성
: 전신 항암화학요법(시스플라틴 기반) 또는 면역항암제(Checkpoint inhibitor).
– 일부 고령자나 수술 불가능 환자에서는 방사선치료 병행.
BCG와 방광암(NMIBC, 비근침윤성)
BCG(Bacillus Calmette-Guérin)는 원래 결핵(Tuberculosis) 예방을 위한 생백신이지만
의외로 방광암, 특히 비근침윤성 방광암(NMIBC) 치료에서도 사용됩니다.
- 방광 안에 암이 얕게 퍼져 있는 경우(NMIBC), 수술로 제거한 뒤에도 재발률이 매우 높기 때문에 추가 치료가 필요합니다.
- 이때 BCG를 방광 안에 직접 주입하면, 이 균이 방광 점막에 염증 반응을 유도합니다.
그러면 면역세포들이 모이면서 암세포까지 함께 공격하게 됩니다. - 쉽게 말해 BCG는 면역 시스템을 자극해 암세포를 제거하는 면역치료입니다.
Q. 왜 하필 BCG인가요?
A. BCG는 ‘면역 자극 능력’이 매우 뛰어난 균이기 때문입니다
BCG는 결핵균 계열의 일종인데, 이 균이 원래 면역계와 활발히 상호작용하는 특징이 있습니다. 특히 T세포, 대식세포, NK세포를 자극해 세포독성 면역을 활발히 유도합니다.
BCG가 생백신이라서 면역계가 실제 감염처럼 인식합니다. 체내에서 면역반응을 아주 강하게 유도하기 때문에 방광점막의 암세포까지 공격할 수 있습니다.
고환암 (Testicular Cancer)
젊은 남성에서 가장 흔한 고형암
통증 없는 고환 종괴
조기 진단 시 완치율 높음
[정의]
고환에서 발생하는 악성 종양으로, 대부분은 배세포종(Germ Cell Tumor)입니다.
[원인/위험요인]
– 잠복고환(cryptorchidism)
– 가족력, 과거 고환암 병력
– 클라인펠터 증후군 등 일부 유전적 소인
[임상양상]
– 통증 없는 단단한 고환 종괴가 대표적입니다.
– 일부 환자에서 둔통, 음낭 불쾌감, 드물게 여성형유방이 동반될 수 있습니다.
[진단]
– 신체검사 및 고환 초음파
– 종양 표지자: AFP, β-hCG, LDH
– CT/MRI를 통한 병기 결정
고환암 영상 소견
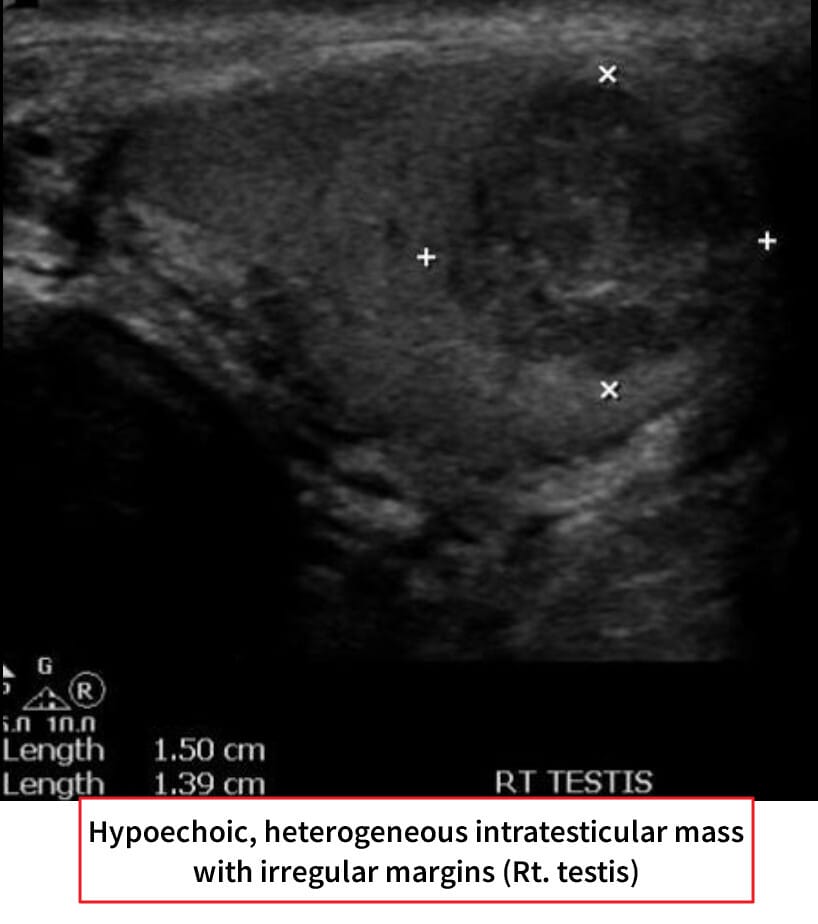
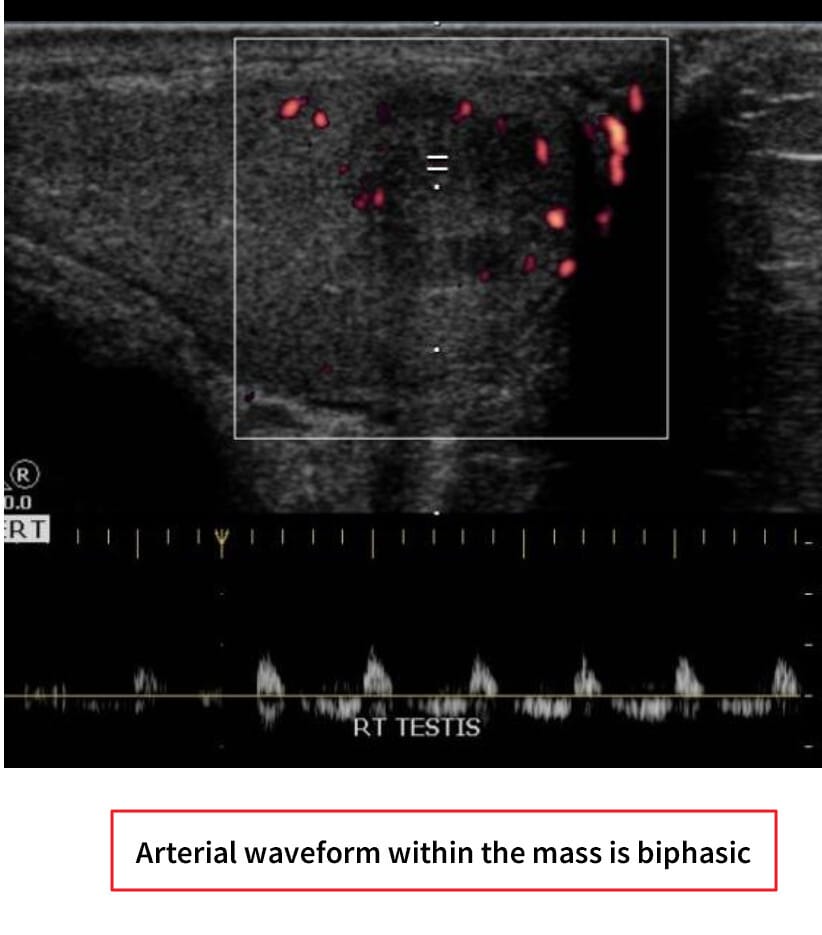
[치료]
– 1차: 근치적 고환 절제술(orchiectomy)
– 병기/조직형에 따른 치료:
A) Seminoma
: 방사선치료·Carboplatin 단일요법 가능
B) Seminoma 아니면
: 항암화학요법(BEP: Bleomycin, Etoposide, Cisplatin) 또는 고용량 요법+조혈모세포이식
– 재발·전이성: 구제 화학요법과 고용량 항암요법 고려
고환암 – Seminoma
– 가장 흔한 고환 생식세포 종양
– 방사선 민감성이 높아 예후가 좋은 편
– 주로 젊은 남성(30~40대)에서 발생
[정의]
– Seminoma는 고환에서 발생하는 대표적인 생식세포 종양(Germ cell tumor)입니다.
– 단일 세포 형태가 균일하고, 방사선 치료에 잘 반응하는 특징을 지니며, 비교적 예후가 좋은 악성 종양입니다.
[원인/위험요인]
– 가장 중요한 위험 요인은 잠복고환(cryptorchidism)입니다.
– 가족력(고환암 병력 있는 형제/부계).
– 고환 발달 이상(Klinefelter syndrome 등).
– 백인에서 상대적으로 높은 발생률.
[임상양상]
– 무통성 고환 종괴
– 진행 시 복부·골반 림프절 전이에 따른 허리 통증이나 복부 종괴.
– 드물게 여성형 유방(호르몬 분비 종양 시)이 동반될 수 있습니다.
[진단]
– 신체검사: 단단한 고환 종괴 촉지.
– 종양표지자: hCG 상승 가능, 그러나 AFP는 정상
– 영상검사: 고환 초음파에서 저에코성 종괴 확인.
– CT/MRI: 병기 설정 및 전이 평가.
– 확진: 고환 절제술(근치적 고환 절제술, radical orchiectomy)을 통한 조직학적 확인.
[치료]
– 치료의 목표는 국소 병변 제거와 전이 억제입니다.
– Seminoma는 방사선과 항암 모두에 잘 반응하여 예후가 좋은 종양군에 속합니다.
1) 1기
: 근치적 고환 절제술 후 적극적 감시, 필요 시 방사선치료 또는 카보플라틴 단일요법.
2) 2기 이상(림프절 전이)
: 절제술 후 방사선치료 또는 시스플라틴 기반 항암화학요법.
3) 전이성
: 항암화학요법(cisplatin, etoposide, bleomycin 조합)이 표준.
전립선암 (Prostate Cancer)
– 서서히 진행하는 경우가 많으며, 초기에는 무증상
– 가장 흔한 형태는 선암(Adenocarcinoma)
– PSA(Prostate-Specific Antigen) 상승이 주요 진단 단서
[정의]
– 전립선 상피세포에서 발생하는 악성 종양으로, 대부분 선암(Adenocarcinoma)
– 서구에서 남성에게 가장 흔한 암 중 하나이며, 한국에서도 고령화로 발생률이 증가하고 있습니다.
[원인/위험요인]
– 가장 중요한 위험요인은 고령입니다 (대부분 65세 이상).
– 가족력, BRCA2 등 유전적 요인.
– 서구화된 식습관(동물성 지방, 고칼로리 식사).
– 호르몬(안드로겐) 의존성이 강해, 남성호르몬이 암 성장에 중요한 역할을 합니다.
[임상양상]
– 초기에는 무증상인 경우가 많습니다.
– 진행 시 배뇨곤란, 잔뇨감, 빈뇨, 야뇨증 같은 하부요로 증상이 나타납니다.
– 골 전이가 흔해 요통, 골통이 나타날 수 있습니다.
– 말기에는 체중감소, 전신 쇠약, 신부전(요로폐쇄) 등이 동반될 수 있습니다.
[진단]
– 혈액검사: PSA(Prostate-Specific Antigen) 상승이 주요 단서.
– 직장수지검사(DRE): 전립선 결절이나 단단한 부위 확인.
– 영상검사: MRI(특히 다매개 MRI, multiparametric MRI)로 국소 병변과 병기 평가.
– 조직검사(Prostate biopsy): gold standard, Gleason score로 분화도와 예후 평가.
– 전이평가: 뼈스캔, CT를 통해 골 전이나 림프절 전이 확인.
[치료]
– 치료의 목표는 암 진행 억제와 환자의 삶의 질 유지입니다.
– 저위험, 국소암: 적극적 감시(active surveillance) 또는 근치적 전립선 절제술(radical prostatectomy), 방사선 치료.
– 국소 진행암: 수술 + 방사선치료 + 호르몬 치료 병행 가능.
– 전이암: 호르몬 치료(안드로겐 차단, Androgen Deprivation Therapy)가 기본.
– 호르몬 저항성 전립선암(castration-resistant prostate cancer, CRPC): 항안드로겐제(enzalutamide, abiraterone), 화학요법(docetaxel), 면역·표적치료 고려.
– 고령자나 동반질환이 많은 경우는 증상 조절 중심의 보존적 치료 선택 가능.
기타 전립선 질환
양성 전립선비대증 (Benign Prostatic Hyperplasia, BPH)
[정의]
노화와 안드로겐 작용에 의해 전립선이 증식하여 하부요로폐색 증상을 유발하는 질환입니다.
[원인/위험요인]
– 고령 남성에서 흔히 발생합니다. (노화가 가장 중요한 원인)
– 남성 호르몬 (안드로겐)의 지속적 작용
– 테스토스테론 대사와 DHT(디하이드로테스토스테론)가 주요 기전으로 작용
[임상양상]
– 배뇨지연, 약뇨, 잔뇨감, 빈뇨, 야간뇨가 대표적입니다.
– 심한 경우 급성 요폐, 반복 요로감염이 발생할 수 있습니다.
[진단]
–직장수지검사(DRE, Digital Rectal Exam): 전립선 크기 확인
– 혈액검사: PSA(Prostate-Specific Antigen) 측정 (암과 감별)
–요속검사(Uroflowmetry): 소변 흐름 확인
-방광초음파: 잔뇨량 평가
[치료]
– 약물:
> 알파차단제(Tamsulosin, 방광출구 저항 감소),
> 5α-환원효소억제제(Finasteride, 전립선 크기 축소)
– 수술: 경요도 전립선 절제술(TURP), 레이저 절제술 등
전립선 비대와 폐쇄 증상 (Urinary Obstruction due to Prostate Enlargement)
[정의]
BPH 또는 전립선암 등으로 인해 하부요로폐색이 발생한 상태입니다.
[임상양상]
– 배뇨곤란, 잔뇨감, 야간뇨, 반복 요로감염
– 심한 경우 급성 요폐·수신증·신기능 저하 발생 가능
[치료]
– 원인 질환에 맞춘 약물·수술적 치료
– 급성 요폐 시 일시적 도뇨관 삽입 후 근본적 치료 시행
기타 요도 및 요관 질환
요관 협착 (Ureteral Stricture)
[정의]
요관이 협착되어 수신증, 신손상을 유발하는 질환입니다.
[치료]
– 내시경적 풍선확장술·스텐트 삽입
– 심한 경우 요관 성형술·재건술
신우요관 이행부 협착 (PUJ Obstruction)
[정의]
신우와 요관 사이 협착으로 수신증·신기능 저하를 초래합니다.
[치료]
소아에서는 수술적 교정(pyelo-plasty)이 필요합니다.
요도 협착 (Urethral Stricture)
[정의]
외상, 감염, 수술 후 흉터로 요도가 좁아진 상태입니다.
[임상양상]
– 세뇨, 잔뇨감, 반복 요로감염
[치료]
– 요도확장술, 내시경 절개술
– 재발 시 요도재건술
요도 게실 (Urethral Diverticulum)
[정의]
요도 주위에 게실이 형성되어 재발성 감염·분비물·통증을 일으키는 질환입니다.
[치료]
– 항생제 치료
– 증상 지속 시 수술적 절제
요도하열 (Hypospadias)
소변 줄기 아래로 분출
조기 수술 교정이 원칙
[정의]
요도구가 음경 끝이 아닌 아래쪽에 위치하는 선천성 기형입니다.
[임상양상]
– 소변 줄기 방향 이상
– 음경 하측 만곡(chordee)
– 성인에서 교정되지 않은 경우 성기능·생식기능 문제
[치료]
– 생후 6~18개월 사이 수술 교정이 권장됩니다.
– 요도 재건술(urethroplasty)을 시행하며, 필요 시 음경 만곡 교정 병행
기타 방광 질환
과민성 방광 (Overactive Bladder, OAB)
절박뇨·빈뇨·야간뇨
행동요법 → 약물 → 보툴리눔/신경조절
잔뇨·폐색 동반 시 주의
[정의]
구조적 원인 없이 절박성 요실금을 동반할 수 있는 저장증상이 지속되는 기능성 질환입니다.
[원인/위험요인]
– 노화·신경계 질환·출산력·카페인/이뇨제 등이 영향을 줍니다.
[임상양상]
– 절박뇨·빈뇨·야간뇨·절박성 요실금이 나타납니다.
[진단]
– 배뇨일지·요검사·잔뇨 확인 후 필요 시 요역동학검사를 시행합니다.
[치료]
– 1단계: 체중조절·카페인 제한·방광훈련을 시행합니다.
– 2단계 약물:
– 항무스카린제: 옥시부티닌·톨테로딘·솔리페나신 등 → 구강건조·변비 모니터링이 필요합니다.
– β3 작용제: 미라베그론·비베그론 → 인지 부작용 적고 고령에 유리합니다.
– 반응 불충분 시 두 군 병용을 고려합니다.
– 3단계: 방광내 보툴리눔 독소, 천경신경 자극(PTNS), 천골신경 조절을 선택합니다.
신경인성 방광 (Neurogenic Bladder)
저장/배출 기능 장애
상부요로 보호 + 요로감염 최소화
자가도뇨가 기본
[정의]
중추·말초 신경 손상으로 방광·괄약근 조절이 장애를 보이는 상태입니다.
[원인/위험요인]
– 척수손상·다발성경화증·당뇨병성 신경병증·뇌혈관질환 등이 원인입니다.
[임상양상]
– 요절박·요실금·요폐가 교대하며, 재발성 UTI가 흔합니다.
[진단]
– 요역동학검사로 순응도·과활동·DSD 여부를 평가합니다.
[치료]
– 기본: 간헐적 자가도뇨(CIC)로 저압 배출을 유지합니다.
– 약물: 항무스카린제 또는 β3 작용제로 저장압을 낮춥니다.
– 난치성: 보툴리눔 독소 방광주입, 천골신경 조절을 고려합니다.
– 고압 방광·상부요로 손상 위험 시 확대방광술 등 재건을 검토합니다.
배뇨 및 소변 이상
혈뇨 (Hematuria)
현미경적 vs 육안적
신장·요관·방광·요도 어디서든 발생
원인 감별이 중요
[정의]
소변에서 적혈구가 검출되는 상태로, 현미경적과 육안적으로 나눕니다.
[원인/위험요인]
– 신장: 사구체신염, 신장암, 다낭신
– 요관: 요로결석, 협착
– 방광: 방광염, 방광암
– 요도: 요도염, 외상
[임상양상]
– 무증상 현미경적 혈뇨는 건강검진에서 흔히 발견됩니다.
– 육안적 혈뇨는 소변 색이 콜라색/선홍색으로 변하며, 통증 유무에 따라 감별 진단이 달라집니다.
[진단]
– 요검사·현미경 검사
– 영상: 신장/방광 초음파, CT urography
– 필요 시 방광경
[치료]
– 원인 치료가 가장 중요합니다.
– 감염성: 적절한 항생제(예: Ciprofloxacin, Ceftriaxone 등)
– 결석성: 수분 공급, α차단제, 필요 시 쇄석술
– 종양성: TURBT(방광암), 신절제술(RCC) 등

