
Table of Contents
골수이형성증후군 (Myelodysplastic Syndromes)
골수이형성증후군(Myelodysplastic Syndromes, MDS)는 조혈모세포의 분화 및 성숙 이상으로 인해 비정상적 혈구가 형성되고, 말초혈액에서 혈구 감소증(cytopenia)이 발생하는 클론성 조혈 질환입니다. 일부 환자는 급성골수성백혈병(AML)으로 진행할 수 있습니다.
- 백혈병 전단계 (Preleukemic condition)으로 간주되는 혈액암 계열의 질환입니다.
비정상적인 조혈세포의 분화로 골수는 과세포성이나, 말초혈액에서는 혈구가 감소하는 ‘무기력한 조혈’이 특징입니다.
| 골수이형성증후군 (Myelodysplastic Syndromes) |
| 🟥 골수 내 조혈세포들이 이형성을 보이며, 말초혈액에서 빈혈, 호중구 감소증, 혈소판 감소증이 나타납니다. |
| ✅ 말초혈액에서 1계통 이상의 cytopenia와 |
| 골수검사에서 이형성세포 ≥10%, |
| 또는 특정 염색체 이상 존재 시 진단합니다. |
원인
대부분 특발성이지만, 항암치료, 방사선 노출 등이 위험 인자로 작용합니다.
| 주요 원인 |
| 🔴 노화 및 체세포 돌연변이 |
| 고령에서 발생률이 증가하며, DNA 손상 축적과 클론성 조혈과 연관됩니다. |
| 🔴 항암화학요법 및 방사선 노출 |
| 이차성 MDS는 치료 관련 유발(t-MDS)로, 예후가 더 불량합니다. |
| 🔴 유전적 질환 |
| Fanconi anemia, Diamond-Blackfan anemia 등 선천성 질환과 관련된 경우도 있습니다. |
증상
혈구 감소증에 따른 증상이 주요하며, 초기에는 무증상일 수 있습니다.
| 주요 증상 |
| 🟨 빈혈 증상 |
| 피로, 창백, 호흡곤란 등 만성 빈혈의 증상이 흔하게 나타납니다. |
| 🟨 출혈 경향 |
| 혈소판 감소로 인한 자반, 코피, 점막 출혈 등이 발생합니다. |
| 🟨 감염 |
| 호중구 감소로 인해 세균·진균 감염에 취약해집니다. |
진단
골수조직 검사와 유전학적 분석을 통해 확진하며, WHO 및 IPSS-R 기준으로 분류합니다.
| 진단 기준 |
| 🔵 골수검사 |
| 골수세포 내 1계통 이상에서 ≥10% 이형성 확인이 필요합니다. |
| 🔵 염색체 이상 |
| del(5q), monosomy 7, trisomy 8 등 |
| 🔵 말초혈액 검사 |
| 비정상 적혈구, 과립구, 거대 혈소판 등이 관찰되며, pancytopenia가 동반됩니다. |
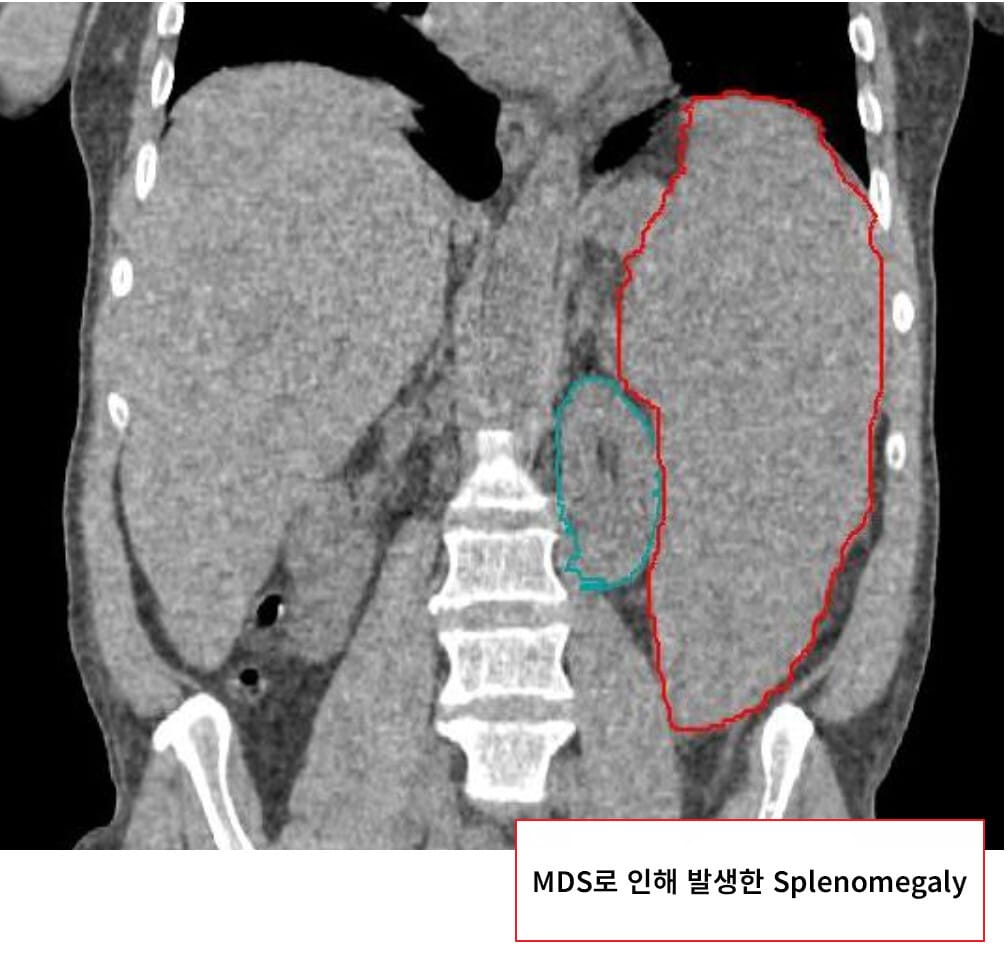
병리소견
골수이형성증후군(MDS)은 조혈모세포의 클론성 이상으로 인해 조혈 전구세포의 분화 및 성숙이 비정상적으로 진행되며, 이로 인해 하나 이상의 혈구 계통에서 이형성이 나타나는 것이 특징입니다.
| 🔴 골수 세포 이형성 |
| 적혈구, 과립구, 거대핵세포 계열에서 모두 이형성(dysplasia)을 보일 수 있으며, 진단 시 10% 이상의 세포에서 이형성이 관찰되어야 합니다. |
| 🔴 적혈구계 이형성 |
| Ring sideroblasts(철적환적혈모구)가 관찰될 수 있으며, 다핵성 또는 핵소체 비정상, 핵-세포질 비례 이상 등도 흔합니다. |
| 🔴 과립구계 이형성 |
| 저세분화된 과립구(hypogranulation), 핵의 이분화, pseudo-Pelger-Huët anomaly(핵이 둘로 나뉜 중성구) 등이 나타납니다. |
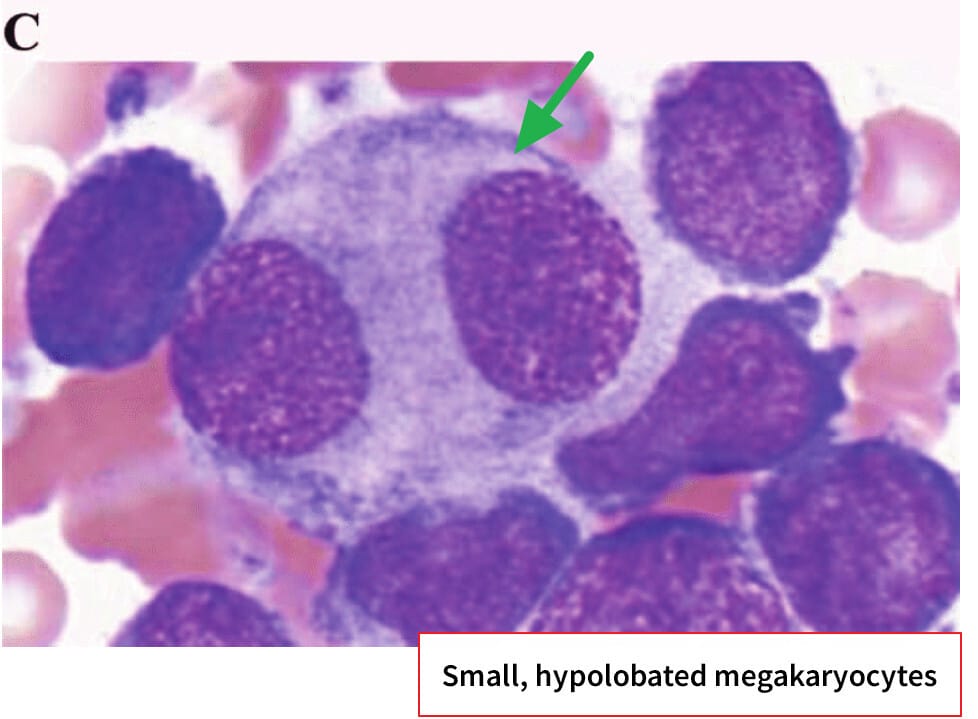
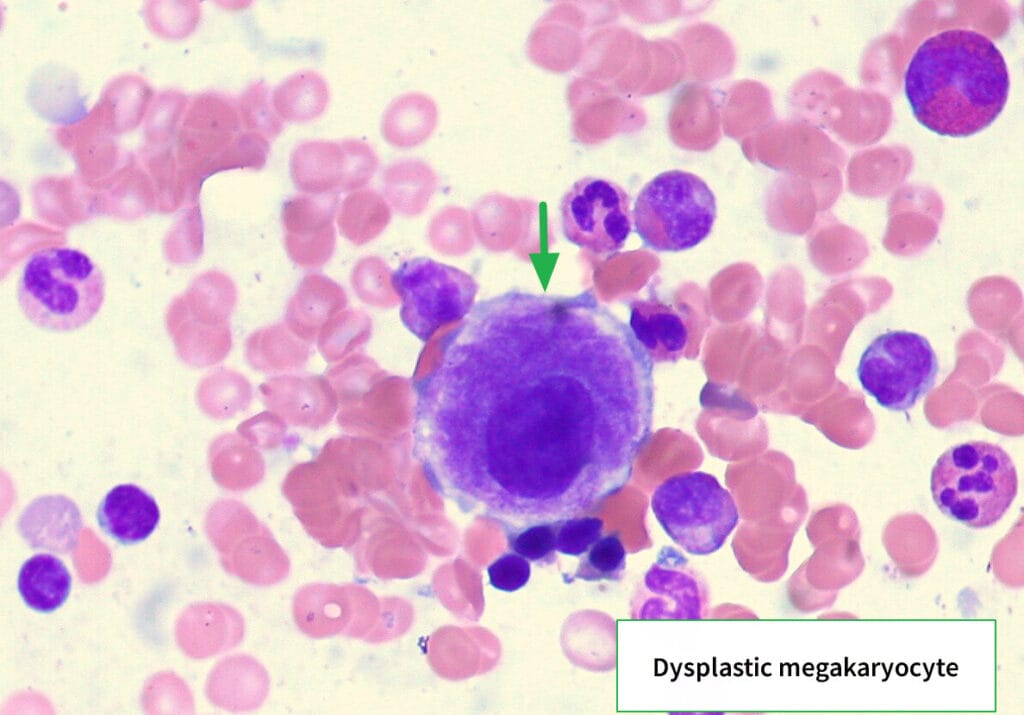
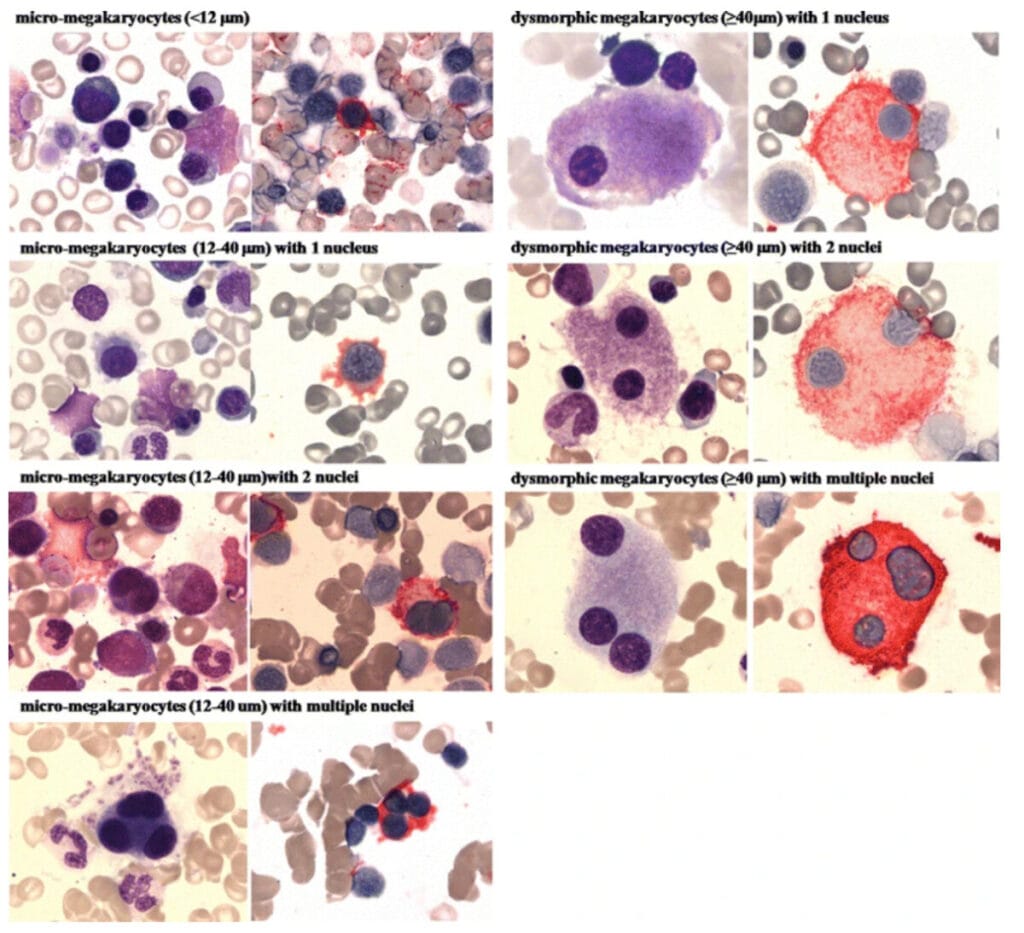
| 🔴 거대핵세포계 이형성 |
| 거대핵세포의 다분열성 및 소형화(micromegakaryocytes), 이핵성 또는 핵 소절화(dispersed nuclear lobation)가 관찰됩니다. |
| 🔴 과형성 또는 저형성 골수 |
| 골수세포가 증가된 경우도 있으나, 일부 아형에서는 저세포성(hypocellular) 골수가 나타나기도 합니다. |
| 🔴 Blast 세포 비율 |
| 골수 내 blast 세포가 20% 미만일 경우 MDS로 진단하며, 20% 이상일 경우 급성 골수성 백혈병(AML)로 진단합니다. |
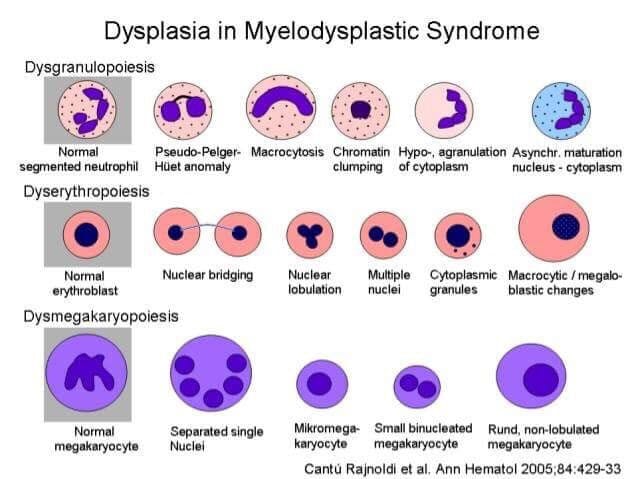
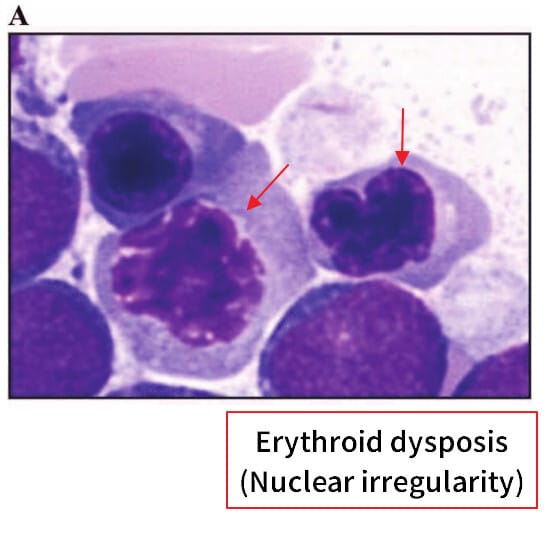
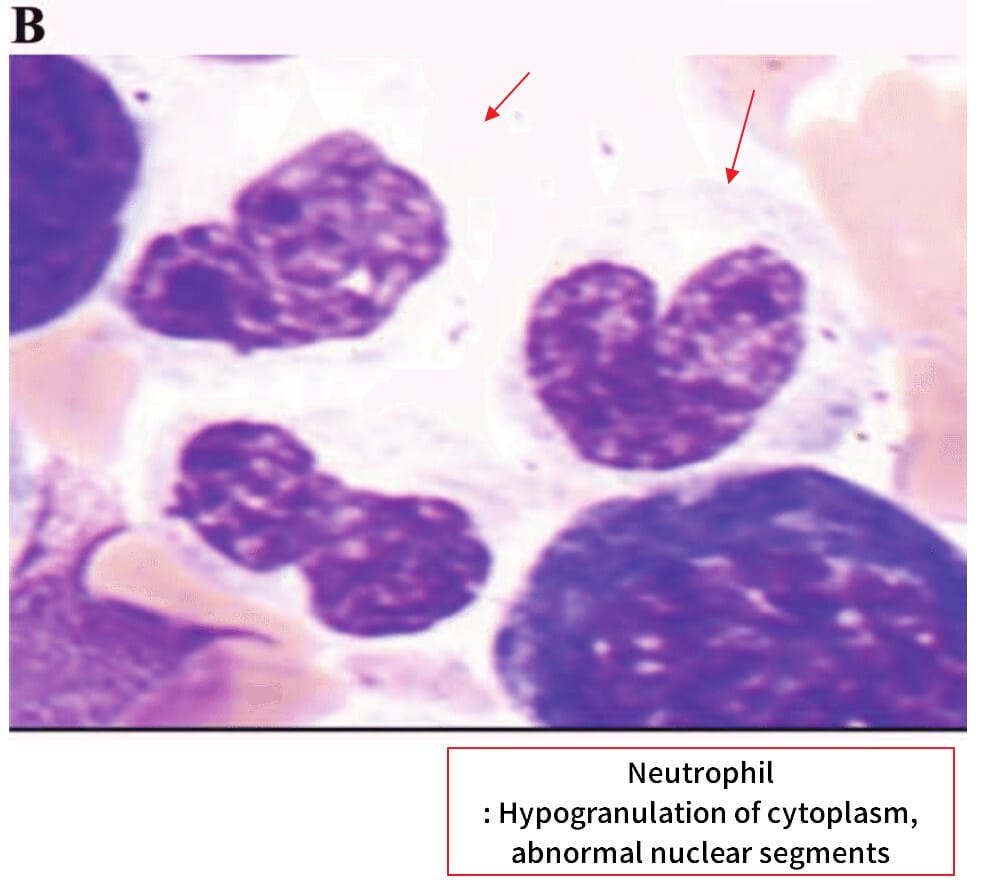
치료
위험도에 따라 치료 방침이 달라지며, 목표는 생존 연장 또는 증상 완화입니다.
Low-risk MDS
| 저위험군 치료 전략 |
| 🔵 관찰 또는 지지 치료 |
| 무증상 환자는 경과관찰하며 필요시 수혈 또는 조혈성장인자(ESA)를 투여합니다. |
| 🔵 Lenalidomide (레날리도마이드) |
| del(5q) 환자에게 특이적으로 효과적이며, 수혈 의존성 개선에 도움을 줍니다. |
High-risk MDS
| 고위험군 치료 전략 |
| 🔵 Azacitidine (아자시티딘) |
| DNA hypomethylating agent로, 생존기간 연장 및 AML 진행 지연 효과가 입증되었습니다. |
| 🔵 Allogeneic HSCT (동종 조혈모세포이식) |
| 유일한 근치적 치료법이며, 젊고 적합한 공여자가 있을 경우 시행합니다. |
예후
Revised IPSS-R (International Prognostic Scoring System)에 따라 예후를 분류합니다.
| 예후 평가 |
| ✅ 골수아세포 비율, 염색체 이상, 혈구 수치에 따라 5등급으로 나누며, 생존율과 AML 전환율이 달라집니다. |


