
Table of Contents
급성 골수성 백혈병 (Acute Myeloid Leukemia, AML)
급성 골수성 백혈병(Acute Myeloid Leukemia)은 골수 내 미성숙 골수모세포(myeloblast)가 비정상적으로 증식하면서 정상 조혈 기능을 억제하고 말초혈액 및 전신 장기에 침윤하는 혈액암입니다.
골수에서 미성숙한 백혈구(골수아세포)가 통제 불능으로 증식하여 정상적인 혈액 세포 생성을 억제하는 혈액암입니다. 진행이 빠르며 (급성), 치료하지 않으면 수개월 내에 생명을 위협할 수 있습니다.

| 급성 골수성 백혈병 (Acute Myeloid Leukemia, AML) |
| ✅ 골수에서 비정상적인 골수아세포가 과도하게 증식하여 정상 혈액 세포 기능을 저해하는 급성 혈액암입니다. |
| ✅ 진단 기준 |
| 골수 또는 말초 혈액에서 골수아세포(myeloblasts)가 20% 이상 발견될 때 진단합니다. |
ALL과의 비교
AML vs ALL
: 표현이 좀 이상하지만 Myeloblast 가 좀 더 널럴해보이고(?) 연합니다.

✅ Myeloblast (골수모세포)
- Cytoplasm이 적당히 있음 (Moderate amount)
- Chromatin이 약간 가늘게 분산되어 있음 (Fine lacecy chromatin)
- Nucleoli가 뚜렷함. 2~5개까지 관찰됨 (Prominent Nucleoli)
- Auer Rod를 포함할 수도 있다!

✅Lymphoblast (림프모세포)
- Cytoplasm이 거의 없다 (Scant amount)
- Chromatin이 조밀하다, 성숙한 형태 (Dense chromatin)
- Nucleoli가 뚜렷하지 않음 . (Indistinct Nucleoli)
- Auer Rod가 있을 수 없다!
원인
다양한 후천적 돌연변이와 유전적 요인이 복합적으로 작용합니다.
| 주요 원인 |
| 🔴 고령(Age) |
| 65세 이상 고령에서 발생 위험이 높습니다. |
| 🔴 화학물질 노출(Chemical exposure) |
| 벤젠, 방사선 등에 노출 시 위험이 증가합니다. |
| 🔴 항암제 후 백혈병(Therapy-related AML) |
| 알킬화제, topo II 억제제 사용 후 수년 내 발생할 수 있습니다. |
| 🔴 유전 질환(Genetic syndromes) |
| 다운증후군, 팬코니 빈혈 등에서 백혈병 위험이 증가합니다. |
| 🔴 골수이형성증후군(MDS) 병력 |
| 기존 골수질환에서 이차적으로 AML로 진행될 수 있습니다. |
임상양상
정상 조혈이 억제되어 빈혈, 감염, 출혈이 주요 증상입니다.
피로, 잦은 감염, 멍이나 출혈이 쉽게 발생하며, 일부 환자는 잇몸 종대나 피부 결절로 나타납니다.
| 증상 및 징후 |
| 🟨 피로, 창백, 호흡곤란 |
| 적혈구 감소로 산소 운반능력이 떨어져 빈혈 증상이 나타납니다. |
| 🟨 잦은 감염 |
| 백혈구는 많지만 기능이 없어 세균, 진균 감염에 취약합니다. |
| 🟨 멍, 출혈 경향 |
| 혈소판 감소로 피부 멍, 코피, 잇몸출혈이 쉽게 발생합니다. |
| 🟨 잇몸비대, 피부결절 |
| 백혈병세포가 잇몸이나 피부에 침윤하여 종괴처럼 보일 수 있습니다. |
진단
골수천자 및 혈액검사를 통해 진단하며, 세포유전학적 이상을 확인해야 합니다.

| 진단 방법 |
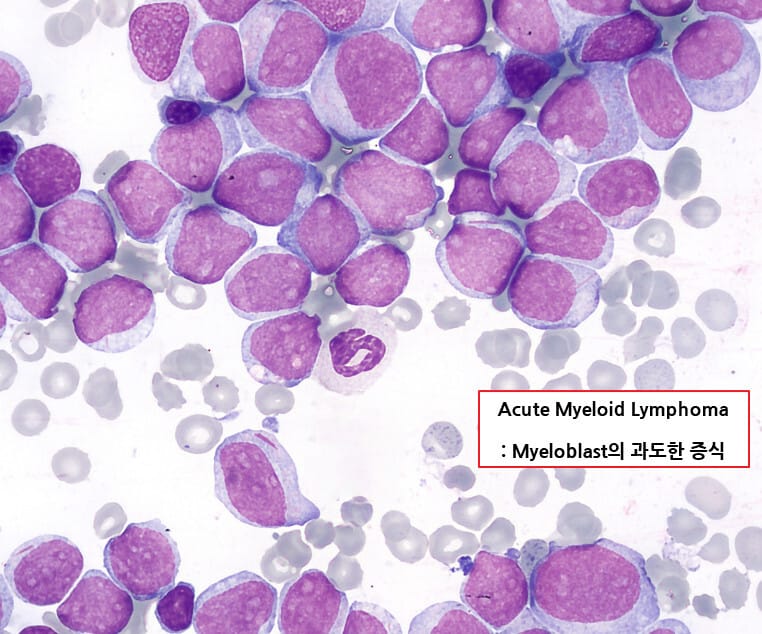
| 🔵 말초혈액 도말(PB smear) |
| 백혈병 모세포(blast)가 보이며, Auer rod가 관찰될 수 있습니다. |
| 🔵 골수천자(Bone marrow aspiration) |
| 골수 내 모세포가 전체 세포의 ≥20% 이상이면 AML로 진단합니다 (WHO 기준). |
| 🔵 면역표현형검사(Flow cytometry) |
| AML에서 흔한 CD13, CD33, MPO 등의 마커를 확인합니다. |
| 🔵 세포유전학(FISH, karyotyping) |
| 염색체 이상(t(8;21), inv(16), t(15;17) 등)을 확인하여 예후와 치료 반응 예측에 사용합니다. |
| 🔵 분자유전학 검사(Molecular study) |
| FLT3, NPM1, CEBPA 등의 유전자 변이 여부를 확인합니다. |
아형 (Subtypes)
FAB(French-American-British) 분류는 골수 형태학에 기반하여 급성 골수성 백혈병을 M0~M7까지 8가지 아형으로 분류합니다.
✅ M3 (APL) 은 유일하게 분화유도요법(ATRA, ATO)으로 치료 가능
🟦 M2, M3, M4Eo 는 좋은 예후 관련 유전자 이상이 동반될 수 있음
🟥 M5, M6, M7 은 조직 침윤이 두드러지며 예후가 불량한 경우가 많음
| 분류 |
| 🟦 M0 — 최소분화형 (Minimally differentiated AML) |
| 형태학적으로 미성숙하여 골수모세포임을 구분하기 어렵고, 면역표현형 검사로 진단합니다. |
| 🟦 M1 — 분화 없음형 (AML without maturation) |
| 모세포가 대부분을 차지하며, 성숙 백혈구 계통으로의 분화가 거의 없습니다. |
| 🟦 M2 — 일부 분화형 (AML with maturation) |
| 모세포 외에도 일부 성숙 백혈구가 관찰되며, t(8;21) 염색체 이상과 관련 있습니다. |
| 🟥 M3 — 전골수구성 백혈병 (Acute Promyelocytic Leukemia, APL) ✨ |
| 전골수구가 우세하며, t(15;17) → PML-RARA 유전자 전좌로 진단. ATRA 및 ATO 치료에 매우 잘 반응합니다. Auer-rods가 두드러지게 나타납니다. |
| 🟦 M4 — 골수단구성 백혈병 (Acute myelomonocytic leukemia) |
| 골수구와 단구 계통이 모두 증식하며, 조직 침윤이 흔하고 gingival hypertrophy가 동반될 수 있습니다. |
| 🟦 M4Eo — 호산구 동반형 (M4 with eosinophilia) |
| inv(16) 또는 t(16;16) 이상 동반. |
| 🟦 M5 — 단구성 백혈병 (Acute monocytic leukemia) |
| 모든 계통이 단구 계열로 분화되어 있으며, 피부, 치은 침윤이 특징입니다. |
| 🟦 M6 — 적혈구성 백혈병 (Acute erythroid leukemia) |
| 골수 세포 중 적혈구 계열 세포가 50% 이상이며, 매우 드물고 예후는 불량한 편입니다. |
| 🟦 M7 — 거대핵모구 백혈병 (Acute megakaryoblastic leukemia) |
| 거대핵세포 계열로 분화된 모세포가 우세. 다운증후군 소아에서 좋은 예후를 보입니다. |
M3 type (Acute Promyelocytic Leukemia, APL)
M3 type은 급성 골수성 백혈병(AML)의 아형 중 하나로, 급성 전골수구성 백혈병(Acute Promyelocytic Leukemia, APL)이라고도 부릅니다. 이 아형은 t(15;17)(q24;q21) 전좌에 의해 발생하며, PML-RARA 유전자 융합이 형성되어 조혈 전구세포의 분화를 저해합니다.
주된 세포는 전골수구(Promyelocyte)로 구성되어 있으며, 이들 세포는 과립이 풍부하고 핵이 주름져 있는 특징을 보입니다. 특히, 골수에서 관찰되는 전골수구는 다수의 Auer rod를 포함하는 경우가 많아 진단에 유용합니다.

APL은 치료하지 않을 경우 심각한 파종성 혈관내 응고(DIC)를 유발할 수 있어 응급 혈액학적 상태로 간주됩니다. 그러나 All-trans Retinoic Acid (ATRA)와 같은 분화 유도제 도입 이후 예후가 크게 향상되었습니다.
치료
M3 (APL)의 치료
AML-M3 (급성 전골수구성 백혈병, APL)은 t(15;17)(q22;q12) 전좌로 인한 PML-RARA 융합유전자가 병인으로, 분화유도치료를 통해 치료 할 수 있습니다.
ATRA (all-trans retinoic acid)와 ATO (arsenic trioxide)를 병용하여 치료합니다. 조기 치료가 생존율을 결정합니다.
분화유도 치료 (Differentiation Therapy)
미성숙한 세포가 성숙한 세포로 ‘분화’하도록 ‘유도’
분화유도 치료는 미성숙한 전골수구(promyelocyte)를 성숙한 과립구로 유도하여, 백혈병세포의 증식을 멈추게 하는 치료입니다. AML-M3 (APL)에서만 적용되며, PML-RARA 융합단백의 작용을 직접적으로 억제합니다.
| 💊 ATRA (All-trans retinoic acid) |
| 전골수구를 성숙한 형태로 분화시켜 백혈병세포를 제거합니다. |
| 💊 ATO (Arsenic trioxide) |
| PML-RARA 단백질을 분해하고 세포사멸을 유도합니다. |
| 위험도에 따른 치료 방향 |
| WBC < 10,000/μL: ATRA + ATO 단독 사용 |
| WBC ≥ 10,000/μL: ATRA + ATO + 항암제(Idarubicin 등) |
| 주의 사항 |
| 🟧 초기 치료 시작 전 또는 중단 시 출혈 위험이 높으며, DIC를 동반하므로 지연 없이 ATRA를 즉시 투여해야 합니다. |
| 🟧 분화증후군(발열, 체중 증가, 호흡곤란, 흉막삼출 등)이 발생할 수 있으며, 고용량 스테로이드로 조기 치료해야 합니다. |
기타 AML 아형의 치료
M0~M2, M4~M7에 해당하는 AML 아형은 모두 공통적으로 ‘유도요법 → 공고요법 → 이식 고려’의 단계로 치료합니다.
완전관해(CR)를 유도한 뒤, 재발을 방지하기 위한 공고요법 및 위험도에 따른 조혈모포 이식을 시행합니다.
유도요법 (Induction Therapy)
가능한 많은 백혈병세포를 제거
유도요법은 AML 진단 직후 시행하는 초기 치료 단계로, 가능한 한 많은 백혈병세포를 제거하여 완전관해(complete remission, CR)를 유도하는 치료입니다.
| 🟧 표준 요법: 7+3 regimen |
| : 7+3 요법(Cytarabine 7일 + Anthracycline 3일) 사용, 완전관해 유도 |
| 💊 Cytarabine 100~200 mg/m² IV for 7 days |
| DNA 합성을 억제하여 빠르게 분열하는 백혈병 세포를 제거합니다. |
| 💊 Anthracycline (Idarubicin 또는 Daunorubicin) IV for 3 days |
| Topoisomerase II 억제를 통해 DNA 복제를 차단하여 세포 사멸을 유도합니다 |
| ✅ 완전관해 기준 |
| 골수 내 백혈병 모세포 < 5%, 혈구 회복(ANC ≥ 1000/μL, PLT ≥ 100,000/μL), 말초혈액에서 모세포 없음 |
공고요법 (Consolidation Therapy)
Complete Remission 후 잔존백혈병세포를 제거
공고요법은 완전관해 달성 후 남아 있는 미세잔존 백혈병세포(minimal residual disease, MRD)를 제거하고 재발을 방지하기 위한 치료 단계입니다.
| 🟦 표준 요법: 고용량 Cytarabine (HiDAC) |
| 💊 HiDAC: Cytarabine 1.5~3 g/m² IV, 하루 2회, 3일간 (4주 간격으로 3~4회 반복) |
| 고용량으로 투여 시 CNS로도 약물이 도달하여 중추신경계 재발 예방에도 효과가 있습니다. |
| 🟧 부작용 모니터링 |
| 시신경염(optic neuritis), 신경독성, 위장관 점막염, 골수억제 등에 주의합니다. |
조혈모세포이식 (Hematopoietic Stem Cell Transplantation, HSCT)
조혈모세포이식은 고위험 또는 재발/불응성 AML 환자에서 장기 생존을 기대하기 위한 치료로, 완전관해 상태에서 시행하는 것이 원칙입니다.
| 적응증 |
| ✅ ELN 기준 Intermediate 이상 위험군 ✅ 재발한 AML ✅ 유도요법 후 불완전한 관해 또는 MRD 양성 |
| 금기 |
| 고령, 장기부전, 감염 조절 실패 등으로 이식 독성을 견디기 어려운 경우 |
| 이식 유형 |
| 🔷 동종 조혈모세포이식 (Allogeneic HSCT) |
| HLA-적합 공여자에게 받은 조혈모세포를 이용하여 백혈병세포 제거 + 면역 재구성 효과를 기대합니다. |
| 🔷 자가 조혈모세포이식 (Autologous HSCT) |
| 자신의 조혈모세포를 보관 후 고용량 항암 치료 후 재주입. 현재는 드물게 시행됩니다. |
예후
염색체 및 유전자 변이에 따라 예후가 달라지며, 연령과 전신 상태도 중요합니다.
| 예후 |
| ✅ 좋은 예후 : M2, M3, M4Eo |
| t(8;21), inv(16), t(15;17)과 같은 특이 염색체 이상이 있는 경우 |
| 🟥 나쁜 예후 : M5, M6, M7 |
| FLT3-ITD 변이, 복잡 핵형 등은 치료 반응이 떨어지고 재발 위험이 높습니다. |
| 🟧 고령 환자 |
| 치료 독성이 높아 완전관해율이 낮고, 이식 적응이 어려운 경우가 많습니다. |
생활 관리
감염 예방, 출혈 주의, 영양 유지 등 지지요법이 매우 중요합니다.
| 생활 관리 수칙 |
| 🟨 손 위생 철저히 하기 |
| 백혈구 기능 저하로 감염에 매우 취약하므로 자주 손을 씻어야 합니다. |
| 🟨 날 음식 피하기 |
| 세균 감염 위험이 높은 음식은 피해야 합니다. |
| 🟨 출혈 주의 |
| 혈소판 수치가 낮을 때는 부딪히거나 베이지 않도록 조심해야 합니다. |


